题目内容
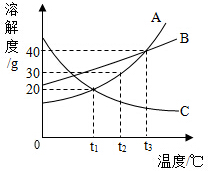 如图是甲、乙、丙三种物质的溶解度曲线图,据图回答下列问题:
如图是甲、乙、丙三种物质的溶解度曲线图,据图回答下列问题:(1)A、B两种物质在
(2)t2℃时,A、B、C三种物质溶解度由大到小排列为
(3)t1℃时,将15gA物质加入到50g水中,充分溶解后,所得溶液是
(4)仅通过改变温度的方法将接近饱和的C溶液转化成饱和溶液应
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法
专题:溶液、浊液与溶解度
分析:(1)根据溶解度曲线焦点表示两种物质的溶解度相等解答;
(2)根据溶解度曲线图解答;
(3)根据t1℃时,A的溶解度为20g解答;
(4)根据C物质的溶解度随温度升高而减小解答.
(2)根据溶解度曲线图解答;
(3)根据t1℃时,A的溶解度为20g解答;
(4)根据C物质的溶解度随温度升高而减小解答.
解答:解:
(1)由溶解度曲线可知t3℃时A物质的溶解度等于B物质的溶解度;
(2)t2℃时,三种物质溶解度由大到小的顺序是B>A>C;
(3)t1℃时,A的溶解度为20g,100g水中最多溶解20g,故将15克A放入50克水中,充分溶解后所得溶液是饱和溶液;
(4)C物质的溶解度随温度升高而减小,要使接近饱和的C溶液变为饱和溶液,可采取的方法有加入溶质C或蒸发溶剂或升温.
答案:
(1)t3
(2)B>A>C
(3)饱和
(4)升温
(1)由溶解度曲线可知t3℃时A物质的溶解度等于B物质的溶解度;
(2)t2℃时,三种物质溶解度由大到小的顺序是B>A>C;
(3)t1℃时,A的溶解度为20g,100g水中最多溶解20g,故将15克A放入50克水中,充分溶解后所得溶液是饱和溶液;
(4)C物质的溶解度随温度升高而减小,要使接近饱和的C溶液变为饱和溶液,可采取的方法有加入溶质C或蒸发溶剂或升温.
答案:
(1)t3
(2)B>A>C
(3)饱和
(4)升温
点评:主要考查了固体溶解度曲线的意义及固体溶解度和温度间的关系,并能灵活利用所学知识来解决实际问题.

练习册系列答案
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
下列变化中,属于化学变化的是( )
| A、干冰升华 | B、海水晒盐 |
| C、糯米酿酒 | D、活性炭吸附 |
下列物质的分类正确的是( )
| A、活泼金属:镁、铝、铜 |
| B、碳单质:金刚石、石墨、C60 |
| C、氧化物:水、氧化铁、熟石灰 |
| D、混合物:纯碱、石油、钢 |
 请回答下列化学与人类生活相关的问题.
请回答下列化学与人类生活相关的问题.