题目内容
3.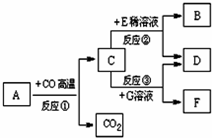 现有A~G七种物质,已知A是赤铁矿的主要成分,B是可燃性气体单质,G溶液为蓝色,它们之间存在如图所示的转化关系:
现有A~G七种物质,已知A是赤铁矿的主要成分,B是可燃性气体单质,G溶液为蓝色,它们之间存在如图所示的转化关系:(1)写出下列物质的化学式:
D:FeSO4; F:Cu;
(2)写出反应的化学方程式
反应①Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
反应③Fe+CuSO4=Cu+FeSO4;
(3)在反应①②③中,属于置换反应的是②③(填序号).
分析 根据题干叙述分析解答,A是赤铁矿的主要成分,故A是氧化铁,氧化铁能与一氧化碳高温反应生成铁和二氧化碳,故C是铁,B是可燃气体单质,故B是氢气,铁能与E的稀溶液反应生成氢气和D,故E可能是稀硫酸,G是蓝色溶液,铁能与G反应生成硫酸亚铁和F,故F是铜,G是硫酸铜溶液,据此解答.
解答 解:A是赤铁矿的主要成分,故A是氧化铁,氧化铁能与一氧化碳高温反应生成铁和二氧化碳,故C是铁,B是可燃气体单质,故B是氢气,铁能与E的稀溶液反应生成氢气和D,故E可能是稀硫酸,G是蓝色溶液,铁能与G反应生成硫酸亚铁和F,故F是铜,G是硫酸铜溶液,带入框图,推断合理;
(1)D是硫酸亚铁,F是铜,故填:FeSO4,Cu;
(2)反应①是氧化铁与一氧化碳高温反应生成铁和二氧化碳,反应③是铁和硫酸铜反应产生硫酸亚铁和铜;故反应的方程式分别为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;Fe+CuSO4=Cu+FeSO4;
(3)反应①是两种化合物的反应,不是置换反应,反应②③是一种单质和一种化合物生成另一种单质和另一种化合物的反应,属于置换反应,故填:②③.
点评 本题为框图式物质推断题,解答本题的关键是根据题干叙述找准解题的突破口,直接得出有关物质的化学式,然后推断得出其他物质的化学式.

练习册系列答案
相关题目
18.在等质量、等质量分数的两份稀硫酸中,分别投入等质量的铁和锌,反应结束后,发现剩余的铁比锌多,则两份溶液中产生的氢气( )
| A. | 放铁的比放锌的多 | B. | 放铁的比放锌的少 | ||
| C. | 一样多 | D. | 无法确定 |
15.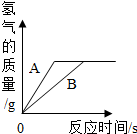 某研究性学习小组分别用等质量的金属Fe和Zn跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如图所示,下列结论中不合理的是( )
某研究性学习小组分别用等质量的金属Fe和Zn跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如图所示,下列结论中不合理的是( )
 某研究性学习小组分别用等质量的金属Fe和Zn跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如图所示,下列结论中不合理的是( )
某研究性学习小组分别用等质量的金属Fe和Zn跟质量相同、溶质质量分数相同的稀硫酸反应,反应生成氢气的质量与时间的关系如图所示,下列结论中不合理的是( )| A. | 反应速率A>B | B. | 可能只有锌剩余 | ||
| C. | 两个反应中硫酸都反应完 | D. | 反应后溶液质量锌大于铁 |
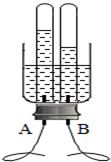 水是“生命之源”,根据你对水的认,请回答:
水是“生命之源”,根据你对水的认,请回答: 化学与生活联系密切,生活中处处有化学.
化学与生活联系密切,生活中处处有化学.