��Ŀ����
���ϵı仯��־�����Ľ����������Ƶò��ϵķ����뻯ѧ��Ӧ�ص���
A. �����մ� B. ��ĥʯ�� C. ұ������ D. �ϳ�����
B ����������ѧ�仯��ָ�仯ʱ�������������ʵı仯�������仯��ָû�������������ʵı仯��A�������մɣ��������������ʣ����ڻ�ѧ�仯��B����ĥʯ����û�������������ʣ����������仯��C��ұ���������������������ʣ����ڻ�ѧ�仯��D���ϳ����ڣ��������������ʣ����ڻ�ѧ�仯����ѡB�� �㾦�������仯�ͻ�ѧ�仯�ı������������������������ɡ� �̲�ȫ���ִʾ�ƪϵ�д�
�̲�ȫ���ִʾ�ƪϵ�д���7�֣�������ʹ�����Ľ������ϡ�
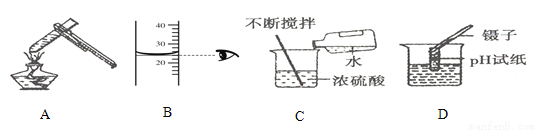
��1����ͼΪʵ����������װ��ͼ��A�з�Ӧ�Ļ�ѧ����ʽ�� ������Ӧ�������ͨ��װ��B��C���ռ��ϴ�����CO��ѭ��ʹ�ã�B��Ӧʢ�ŵ��Լ��� Ũ��Һ��

��2����ҵ�Ͽ�������ϴ��ʴ�Ľ��������������Ƭ�������ͭƬ[ͭ��ijɷ�Cu2(OH)2CO3]ͬʱ����һ���������У����ܷ����Ļ�ѧ��Ӧ�У�
��ͭ���ܡ�������
Cu2(OH)2CO3+ 4HCl= 2CuCl2 + 3X + CO2������X�Ļ�ѧʽΪ ��
�������ܡ�������
��ѧ����ʽΪ ��
���н����������ɣ���ѧ����ʽΪ ��
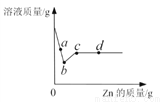
��3��ij��ѧС�����ⶨһ�ָ���Ʒ�����ĺ�����ʵ�������ͼ��ʾ��ʵ������¼���±���

��Ӧʱ�� | t0 | t1 | t2 | t3 |
�ձ���ҩƷ����/g | 55.7 | 55.6 | 55.5 | 55.5 |
�پ����㣬���ָ���Ʒ�����ĺ����� % (��ȷ��0.1��)��
����ͬѧ��������տ�ʹ���е�̼ת��Ϊ������̼������Ʒ��������ᡣ�������ǽ�һ�����ĸ���Ʒ���պ����������������ˣ���ԭ���� ��
��1��3CO + Fe2O3 3CO2 +2 Fe �������ƣ���NaOH�� ��2����H2O �� Fe2O3 + 6HCl = 2FeCl3 + 3H2O �� CuCl2 + Fe = Cu + FeCl2 ��3����98.2�� �ڸ��к�̼���٣�����̼���ٵ�������ԶС����ת��Ϊ������ʱ���ӵ����� �������� �����������1��һ����̼��ԭ�������ķ�Ӧ����ʽΪ��3CO + Fe...��ȥ���������е����ʣ������Լ��ͷ�������ȷ����
���� | ���� | �������õ��Լ��ͷ��� | |
A | ���� | ���� | ľ̿����ȼ |
B | ϡ���� | ϡ���� | �����������Ȼ�����Һ������ |
C | ����������Һ | ����������Һ | ����������̼������Һ������ |
D | �Ȼ��� | ����� | ���������������̣����� |
A. A B. B C. C D. D
C ��������A��ľ̿�������ڵ�ȼ������Ӧ���ɶ�����̼���壬�ܳ�ȥ���ʵ��������µ����ʶ�����̼�������ϳ���ԭ����B��H2SO4����������BaCl2��Һ��Ӧ�������ᱵ���������ᣬϡ��������Ȼ�����Ӧ���������ܰ����ʳ�ȥ�������ԭ���ʳ�ȥ�������ϳ���ԭ����C������������Һ����������̼������Һ��Ӧ����̼��Ƴ������������ƣ��ܳ�ȥ������û�������µ����ʣ����ϳ���ԭ����ȷ��D��KClO3...