题目内容
5.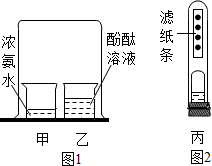 某同学对教材中探究分子性质的实验(图1)进行了改进,如图2所示,试管丙中有一张每隔1厘米滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的敞口小药瓶固定在橡皮塞上. 关于图1、图2中的实验有以下说法,其中错误的是( )
某同学对教材中探究分子性质的实验(图1)进行了改进,如图2所示,试管丙中有一张每隔1厘米滴有一滴酚酞溶液的滤纸条,装有适量浓氨水的敞口小药瓶固定在橡皮塞上. 关于图1、图2中的实验有以下说法,其中错误的是( )①图2比图1的实验更环保、更节约;
②图2中观察到的现象是滤纸条上的酚酞试液自上而
下依次变红;
③将图2中的浓氨水换成浓盐酸,也可达到实验目的;
④若另取与丙相同的装置浸入热水中与丙做对比实验,
可得出分子运动速率与温度有关的结论.
| A. | ①② | B. | ②④ | C. | ②③ | D. | ③④ |
分析 本题考查了分子的性质,结合分子在不断地运动,同种分子性质相同,不同种分子性质不同来分析解答.
解答 解:①图2实验是在密封的小容器内进行的,与图1比较更环保、更节约,故正确;
②由于分子在不断地运动,所以看到滤纸条上的酚酞试液自下而上依次变红,故错误;
③盐酸不能使无色酚酞试液变色,故错误;
④分子在不同温度下都是在不断运动的,温度越高,分子运动速率越大,故正确.
故选C.
点评 首先分析该题考查的知识点,然后结合所学的知识进行解答,该题题型新颖,培养了学生灵活运用知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.将15g镁、铁、锌混合物放入200g稀硫酸中恰好完全反应,然后对所得混合溶液在无氧条件下进行蒸发,得到63g不含结晶水的固体.则所用稀硫酸的溶质质量分数为( )
| A. | 4.9% | B. | 9.8% | C. | 19.6% | D. | 24.5% |
16.将以下物质分别放入足量水中,不能形成溶液的是( )
| A. | 食盐 | B. | 白糖 | C. | 胆矾 | D. | 冰块 |
13.松雷中学化学兴趣小组的同学想测定某建筑工地大理石废料中碳酸钙的含量,做了如下实验:首先称取8g该大理石样品放入烧杯中,然后将40g的稀盐酸分4次加入(假设其余杂质均不与盐酸反应也不溶于水)进行充分反应.实验过程中的数据记录如下:
(1)X的值3.
(2)写出实验中发生反应的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)列出求解生成二氧化碳总质量的比例式$\frac{100}{8g-1.2g}$=$\frac{44}{x}$.
(4)样品中碳酸钙的质量分数是85%.
(5)要想制得280t含杂质15%的生石灰,需要这种大理石废料的质量为500t.
| 次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 稀盐酸的质量 | 10g | 10g | 10g | 10g |
| 剩余固体质量 | 5.5g | X | 1.2g | Y |
(2)写出实验中发生反应的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
(3)列出求解生成二氧化碳总质量的比例式$\frac{100}{8g-1.2g}$=$\frac{44}{x}$.
(4)样品中碳酸钙的质量分数是85%.
(5)要想制得280t含杂质15%的生石灰,需要这种大理石废料的质量为500t.
20.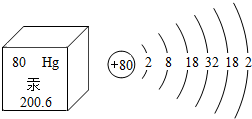 如图为汞元素的信息,下列说法正确的是( )
如图为汞元素的信息,下列说法正确的是( )
 如图为汞元素的信息,下列说法正确的是( )
如图为汞元素的信息,下列说法正确的是( )| A. | 汞的中子数为80 | |
| B. | 汞属于非金属元素 | |
| C. | 汞的相对原子质量为200.6g | |
| D. | 在化学反应中,汞原子容易失去电子 |
10.能造成酸雨的气体是( )
| A. | 二氧化碳 | B. | 一氧化碳 | C. | 氮气 | D. | 二氧化硫 |
17.甲烷和水反应可以制水煤气(混合气体),其反应的微观示意图如图所示.根据微观示意图得出的结论正确的是( )
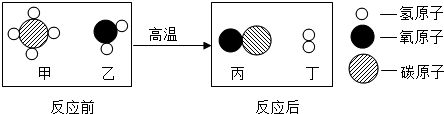

| A. | 反应前后各元素的化合价均不变 | |
| B. | 该反应中含氢元素的化合物有3种 | |
| C. | 该反应中乙和丁的质量比为3:1 | |
| D. | 该反应中丙和丁的分子个数比为1:3 |
14.下列实验现象描述正确的是( )
| A. | 硫在氧气中燃烧,产生淡蓝色火焰 | |
| B. | 镁条在空气中燃烧,发出耀眼白光 | |
| C. | 铜片放入稀硫酸中,有气泡产生 | |
| D. | 一氧化碳还原氧化铁,固体粉末由黑色变为红色 |
13.下列有关实验现象的描述正确的是( )
| A. | 铁丝在空气中燃烧时火星四射,有黑色四氧化三铁固体生成 | |
| B. | 镁条在盛有盐酸的试管中剧烈反应,产生大量气泡,试管壁发烫 | |
| C. | 一氧化碳还原氧化铁时,红棕色粉末逐渐变为银白色 | |
| D. | 打开浓盐酸的瓶塞,瓶口出现大量白烟 |