题目内容
5.科学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:查资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其他成分遇到盐酸时无气体产生.牙膏样品中碳酸钙的定量测定:取适量牙膏样品,利用如图所示
装置进行实验(图中夹持仪器略去),充分反应后,测定C装置中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
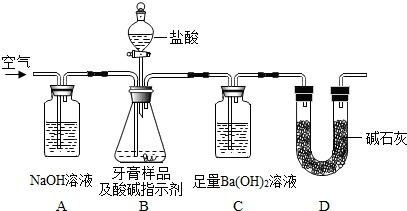
请依据实验过程回答下列问题:
(1)实验过程中需持续缓缓通入空气,其目的是把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收.
(2)有人认为不必测定C装置中生成的BaCO3质量,只要测定C装置在吸收CO2前后的质量,同样可以算出碳酸钙的质量分数.实验证明按此方法测定的结果明显偏高,原因是B中的水蒸气、氯化氢气体等进入装置C中,造成质量偏大.
(3)实验中准确称取8.00g样品三份,进行三次测定,测得BaCO3平均质量为3.94g.则样品中碳酸钙的质量分数为多少?
分析 (1)实验通过C装置生成的碳酸钡的质量测定二氧化碳的质量,进而计算牙膏中碳酸钙的质量分数.装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏小;
(2)装置B中的水蒸气和氯化氢气体会进入装置C中;
(3)根据碳酸钙与盐酸反应生成二氧化碳,二氧化碳与氢氧化钡生成碳酸钡沉淀可建立碳酸钙与碳酸钡的关系式,利用题干中的质量关系解决即可.
解答 解:(1)装置中残留部分二氧化碳,不能被完全吸收,导致测定的碳酸钡的质量偏小,持续缓缓通入空气的作用为:把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收,
故答案为:把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收;
(4)B中的水蒸气、氯化氢气体等进入装置C中,导致测定二氧化碳的质量偏大,测定的碳酸钙的质量偏大,碳酸钙的质量分数偏高.
故答案为:B中的水蒸气、氯化氢气体等进入装置C中,造成质量偏大;
(3)由于碳酸钙与盐酸反应生成二氧化碳,二氧化碳与氢氧化钡生成碳酸钡沉淀的方程式分别是:CaCO3+2HCl═CaCl2+H2O+CO2↑;Ba(OH)2+CO2═BaCO3↓+H2O,所以可建立CaCO3→CO2→BaCO3的关系式;
设碳酸钙的质量分数为x
CaCO3→CO2→BaCO3
100 197
8g×x 3.94g
$\frac{100}{8g×x}$=$\frac{197}{3.94g}$
x=25%
故答案为:25%
点评 本考点属于实验方法和过程的探究,根据物质的化学性质根据所掌握的反应认真分析,既要把握实验设计的每步中的实验目的,又要分析数据的误差.

练习册系列答案
 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
13.2014年10月3日~10月12日,第45届世界杯体操赛在南宁举行.运动员在比赛之前常用“镁粉”搓手,某校化学兴趣小组的同学在老师的指导下对“镁粉”的成分进行检测,发现其中不仅含有镁元素,还有碳、氧两种元素,则该“镁粉”不可能是( )
| A. | 纯净物 | B. | 混合物 | C. | 单质 | D. | 化合物 |
8.水的污染原因有如下说法:①工业生产中废渣、废液的任意排放;②城市生活污水的任意排放;③农业生产中农药、化肥的大量施用;④发展淡水养殖业;⑤冰川融化.其中合理的说法是( )
| A. | ①②③④ | B. | ①②③ | C. | ④⑤ | D. | ①②③④⑤ |
5.某课外活动小组为了测定铜铁合金中铁的质量分数,现取铜铁合金样品20.0g,将80.0g稀硫酸平均分成四份,分四次逐渐加入到样品中,每次充分反应后测的剩余固体质量见下表:
试求:
(1)20.0g铜铁合金中,铜的质量为13g.
(2)铜铁合金中,铁元素的质量分数为35%.
(3)20.0g稀硫酸溶液中溶质的质量分数.
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸质量/g | 20.0 | 20.0 | 20.0 | 20.0 |
| 剩余固体质量/g | 17.2 | 14.4 | 13.0 | 13.0 |
(1)20.0g铜铁合金中,铜的质量为13g.
(2)铜铁合金中,铁元素的质量分数为35%.
(3)20.0g稀硫酸溶液中溶质的质量分数.