题目内容
1. 在生产生活中,你会发现“化学就在身边”.
在生产生活中,你会发现“化学就在身边”.(1)刚刚装修的房子由于材料中含有害物质甲醛(CH2O),一进门就会感觉刺眼,为了减少危害,通常会在家中放置一些活性炭,这是利用活性炭的吸附作用.
(2)食醋中含有醋酸(CH3COOH),醋酸属于有机物(填“有机物”或“无机物”),打开瓶盖,会闻到一股酸味,这是由于醋酸易挥发,醋酸溶液的pH<7(填“<、>或=”);
(3)2012年4月19日,以“创新未来”为主题的北京国际车展盛大开幕.自主品牌的中坚力量,江淮展出了同悦电动轿车,永磁直流无刷电机的搭载以及磷酸铁锂电池的使用,将该车与传统车完全区别开来-用电力驱动代替燃油.请回答:
①图中属于金属材料的有②或③.[填序号(1个即可)]
②用铝合金轮毂要比铁制更耐腐蚀,因为铝表面会形成一层致密的氧化物膜,阻止铝进一步被氧化;设计一个实验比较铝、铁金属活动性顺序(也可用化学方程式表示)将铁条插入氯化铝溶液中,无变化(或将铝条插入氯化亚铁溶液中,铝条变黑).
③纯电动车较传统燃油汽车的优点是减少汽车尾气的污染等.
分析 (1)根据分子是运动的、活性炭有吸附性分析回答;
(2)根据醋酸组成、性质分析;
(3)金属材料包括纯金属以及它们的合金;根据金属铝的化学性质进行分析解答;根据金属活动性顺序表的应用:排在金属活动性顺序中前面的金属一般能把排在后面的金属从其盐溶液里置换出,据此进行分析解答.根据传统燃油汽车会产生大量的空气污染物,如一氧化碳、二氧化硫等,据此进行分析解答
解答 解:(1)由于分子是运动的,甲醛的分子通过运动能分散到整个室内,所以,一进门就会感觉刺眼;由于活性炭有吸附性,能吸附甲醛分子,减少危害;故填:吸附作用;
(2)醋酸(CH3COOH)是含有碳元素的化合物,属于有机物,打开瓶盖,会闻到一股酸味,这是由于醋酸易挥发,醋酸溶液呈酸性,溶液的pH<7;故填:有机物;醋酸易挥发;<;
(3)①金属材料包括纯金属以及它们的合金,图中标示物中②镀铬不锈钢、③铝合金轮毂属于金属材料.故填:②或③;
②用铝合金轮毂要比铁制更耐腐蚀,是因为铝在空气中能与氧气反应,其表面生成一层致密的氧化铝薄膜,阻止铝进一步被氧化.
比较铝、铁金属活动性顺序强弱,一般用金属铝与铁的盐溶液或铁与铝的盐溶液,根据能否发生置换反应来判断两者的金属活动性.如将铁条插入氯化铝溶液中,无变化,说明铝的金属活动性比铁强;或将铝条插入氯化亚铁溶液中,铝条变黑,说明铝的金属活动性比铁强等.故填:铝表面会形成一层致密的氧化物膜,阻止铝进一步被氧化;将铁条插入氯化铝溶液中,无变化(或将铝条插入氯化亚铁溶液中,铝条变黑)(其他合理均可);
③从环保的角度分析,传统燃油汽车会产生大量的空气污染物,如一氧化碳、二氧化硫等,电动车较传统燃油汽车有以下优点,可以减少汽车尾气的污染、噪声污染等.故填:减少汽车尾气的污染等(其他合理均可).
点评 化学与我们的生活息息相关,与生产、生活相关的知识是中考考查的热点之一,灵活运用所学知识(金属材料、合成材料、金属活动性顺序等)是正确解答本题的关键.

| A. | S→SO2→Na2SO4→NaOH | B. | HCl→NaCl→CaCl2→HCl | ||
| C. | CO2→Na2CO3→CaCO3→CO2 | D. | Fe→Fe2O3→FeSO4→Fe |
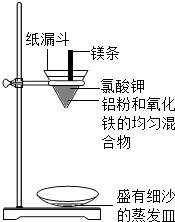 实验二:铝粉和氧化铁粉末反应(铝热反应)
实验二:铝粉和氧化铁粉末反应(铝热反应)实验装置如图:
图中纸漏斗由两张滤纸折叠成漏斗状套在一起,使四周都有四层,点燃镁条后观察到的现象:镁条剧烈燃烧,发出耀眼的白光,放出大量的热,纸漏斗的下部被烧穿,有熔融物落入细沙中.
实验后老师作了如下提示:实验中镁条和氯酸钾的作用是提供反应所需的高温条件,铝粉和氧化铁粉末在高温条件下的反应叫铝热反应,属于置换反应,该反应常用于焊接钢轨.请写出该反应的化学方程式2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al2O3.该反应中单质铝与一氧化碳有相似的还原(填“氧化”或“还原”)性.
实验后同学们对金属与金属氧化物间的反应产生兴趣,激发了探究热情.
【提出问题】任何金属与金属氧化物在高温条件下都能反应吗?
同学们在请教老师后设计了如下实验方案并进行了探究.
【实验方案】
| 实验组别 | 实验操作 | 实验现象 | 结论 |
| 实验1 | 取Zn、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 黑色粉末变成红色 固体部分溶解,有气泡产生,水溶液呈无色. | Zn和CuO能发生置换反应. |
| 实验2 | 取Mg、CuO粉末的均匀混合物于密闭容器中,高温加热. 向冷却后的固体中加入足量的稀盐酸. | 发生爆炸,黑色粉末变成红色. 固体部分溶解,有气泡产生,水溶液呈无色. | Mg和CuO能反应 |
| 实验3 | 取Cu、Fe2O3粉末的均匀混合物于密闭容器中,高温加热. | 粉末无变化 | Cu、Fe2O3不能反应. |
【反思拓展】金属与金属氧化物在高温条件下反应的规律和金属与盐溶液的反应相似.
①15ml量筒 ②10ml量筒 ③20ml量筒 ④胶头滴管.
| A. | ③④ | B. | ①④ | C. | ②④ | D. | ①②④⑤ |
| A. | 人在长跑时急促呼吸 | B. | 铁丝生锈 | ||
| C. | 用秸秆、杂草发酵制沼气 | D. | 酒精燃烧 |