题目内容
9. 水是生命之源,水和溶液在生产生活中起着十分重要的作用.
水是生命之源,水和溶液在生产生活中起着十分重要的作用.(1)家庭里使用的净水器中加入活性炭,所起的作用是吸附.
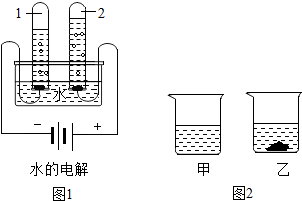
(2)如图1实验过程中,试管1中产生的气体是氢气,从实验中可得出水是由氢元素和氧元素组成的结论.
(3)水是常用的溶剂.如表是氯化钠和氯化铵在不同温度的溶解度.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| NH4Cl | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 | |
②40℃时向两个分别盛有45g氯化铵和氯化钠的烧杯中各加入100g水,充分溶解后,结果如图2所示.则乙烧杯中的溶质是氯化钠.
下列关于甲、乙两烧杯的说法中,正确的是C(填宇母序号)
A、烧杯甲中溶液是饱和溶液
B、烧杯乙中溶液溶质质量分数为31%
C.将烧杯甲中溶液降温到20℃时,溶液中溶质质量分数一定减小
D、升高温度或增加溶剂的量都有可能将烧杯乙中固体全部溶解.
分析 (1)根据活性炭具有吸附性进行解答;
(2)根据水通电分解生成氢气和氧气进行解答;
(3)利用溶质质量=溶液质量×溶质的质量分数,可根据溶液的质量和溶质的质量分数计算配制溶液所需要的溶质的质量.
(4)根据NaCl、NH4Cl在40℃时的溶解度计算分析加入的物质.根据氯化铵和氯化钠在不同温度下的溶解度分析判断有关的说法.
解答 解:(1)活性炭具有吸附性,所以净水器中经常使用活性炭,主要利用活性炭的吸附性;故填:吸附;
(2)水通电分解中,试管1中产生的气体较多,是氢气,试管2中产生的气体较少,是氧气,水通电生成氢气和氧气,从实验中可得出水是由氢元素和氧元素组成的;
(3)溶质质量=溶液质量×溶质的质量分数,配制溶质的质量分数为16%的氯化钠溶液50g,需氯化钠的质量=50g×16%=80g.
设需要再加NaCl的质量是x,
$\frac{200g×8%+x}{200g+x}×$100%=16%
x=19g
(4)由氯化铵和氯化钠在不同温度下的溶解度可可知,在40℃时,氯化铵和氯化钠的溶解度分别是45.8g、36.6g,由图示可知,乙、甲烧杯中的物质完全溶解,则甲烧杯的物质为氯化铵.乙烧杯中的溶质是氯化钠;
A、由于在40℃时,氯化铵的溶解度是45.8g,所以,40℃时,向盛有45g NH4Cl和的烧杯中,加入100g水,充分溶解后,烧杯甲中溶液是不饱和溶液.故A错误;
B、由于在40℃时,氯化钠的溶解度是36.6g.所以,40℃时,向盛有45g氯化钠的烧杯中,加入100g水,充分溶解后,烧杯甲中溶液是饱和溶液,只能溶解36.6g,甲中溶质的质量分数为:$\frac{36.6g}{100g+36.6g}$×100%=26.9%.故B错误;
C、由于在20℃氯化铵的溶解度是37.2g,所以,将烧杯乙中溶液降温至20℃时,溶液中溶质的质量分数一定减小.故C正确;
D、由氯化钠在不同温度下的溶解度可知,在100℃,氯化钠的溶解度是39.8g,所以,升高温度不可能将烧杯甲中固体全部溶解.故D错误.
答案:
(1)吸附;
(2)氢气;氢元素和氧元素;
(3)8;19;
(4)氯化钠;C
点评 本题难度不大,掌握溶质质量分数的有关计算并能灵活运用是正确解答本题的关键.此题是对物质溶解度的考查,解决的重点是能理解溶解度的概念,并能利用溶解度分析并解决问题,属基础性知识考查题.

| A. | O2 | B. | TiO2 | C. | K2CO3 | D. | C6H12O6 |
| A. | 钋原子的原子核外有84个电子 | B. | 钋原子的原子核内有209个中子 | ||
| C. | 钋原子的核电荷数为125 | D. | 钋原子的质量为209g |
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | H2 | HCl | 先通过NaOH溶液,再通过浓硫酸 |
| B | CO | C02 | 通过碱石灰(CaO和NaOH固体) |
| C | C | Fe | 加入过量的稀盐酸,过滤,洗涤,干燥 |
| D | NaOH瑢液 | Na2CO3溶液 | 加入稀盐酸至不再产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 硫酸铜 | B. | 金刚石 | C. | 水 | D. | 氢氧化钠 |
| A. | 用灼烧法鉴别棉花和羊毛 | |
| B. | 用蒸馏水鉴别氢氧化钠固体和硝酸铵固体 | |
| C. | 用带火星的木条鉴别空气和氧气 | |
| D. | 用品尝的方法鉴别稀盐酸和氯化钠溶液 |