题目内容
5.几年前,广西河池宜州市境内龙江河发生了镉浓度超标事件.根据该事件某化学活动小组开展了一次关于金属镉与铜、银活动顺序的探究及镉污染事故处理方法的研讨活动.查阅资料:①镉(Cd)是一种银白色金属,在化合物中通常表现为+2价;
②水体中镉元素通常以氯化镉的形式存在;
③氯化镉能溶于水,氢氧化镉难溶于水.
(一)金属镉与铜、银活动性顺序的探究
| 实验步骤 | 实验现象 | 实验结论 |
| 分别取适量镉、铜、银于试管中,加入足量稀盐酸 | 镉表面有气泡产生,铜、银表面无气泡产生 | 镉的活动性顺序大于铜与银 |
| 取适量铜于试管中,加入少量硝酸银溶液 | 铜表面析出了一层银白色物质, 溶液由无色变为蓝色. | 铜的活动性顺序大于银 |
(二)对镉污染事故处理方法的讨论
小聪认为可用向受污染河段抛撒过量烧碱固体的方法除去氯化镉,反应原理用化学方程式表示为CdCl2+2NaOH═Cd(OH)2↓+2NaCl.小敏认为该方案虽然有效,但有缺陷,原因是烧碱具有强腐蚀性.受小聪与小敏启发,你认为可以用熟石灰(写俗称)代替烧碱.
分析 (一)活泼金属可以和稀盐酸或是稀硫酸反应生成氢气,可以加据此结合金属活动性顺序的应用来解答;
(二)氯化镉可以和碱反应生成沉淀,但是烧碱价格较高,且腐蚀性较强,所以使用熟石灰更合理,可以据此解答.
解答 解:(一)取适量镉、铜、银于试管中,加入足量稀盐酸或是稀硫酸,可观察到镉表面有气泡产生,铜、银表面无气泡产生,从而判断镉的活动性顺序大于铜与银;然后将适量铜于试管中,加入少量硝酸银溶液,观察到铜表面产生了银白色物质,溶液由无色变为蓝色,从而可以判断铜的活动性比银强;
(2)根据题意可以知道氯化镉可以和烧碱溶液反应生成生成氢氧化镉沉淀,该反应的化学方程式为:CdCl2+2NaOH═Cd(OH)2↓+2NaCl;但是氢氧化钠具有强腐蚀性,所以可以用熟石灰来代替烧碱溶液.
故答案为:(一)
| 实验步骤 | 实验现象 | 实验结论 |
| 取适量镉、铜、银于试管中,加入足量的稀盐酸(或稀硫酸) | 镉表面有气泡产生,铜、银表面无气泡产生 | 镉的活动性顺序大于铜与银 |
| 取适量铜于试管中,加入少量硝酸银溶液 | 铜表面析出了一层银白色物质, 溶液由无色变为蓝色. | 铜的活动性顺序大于银 |
点评 解答这类题目时,首先,要熟记和理解金属活动性顺序及其应用,以及与之相关的知识等;然后,根据所给问题情景结合所学的相关知识和技能,细致地阅读、分析题意等细心地进行探究、推理,最后,按照题目的要求,认真地进行选择或解答即可.

练习册系列答案
相关题目
20.分析处理图表中的信息是学习化学的一种重要方法. 如表是KNO3、NaCl在不同温度下的溶解度(单位:g)
(1)20℃时,NaCl的溶解度是36g;
(2)30℃时,KNO3溶液的最大浓度(溶质质童分数)为$\frac{45.8g}{100g+45.8g}$×100%(只列计算式,不需要计算结果);
(3)KNO3中含少最氯化钠时.提纯硝酸钾的一般方法是冷却热饱和溶液;
(4)根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是36g~36.3g.
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
(2)30℃时,KNO3溶液的最大浓度(溶质质童分数)为$\frac{45.8g}{100g+45.8g}$×100%(只列计算式,不需要计算结果);
(3)KNO3中含少最氯化钠时.提纯硝酸钾的一般方法是冷却热饱和溶液;
(4)根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是36g~36.3g.
15.下列实验操作中,正确的是( )
| A. | 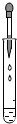 滴加液体 | B. | 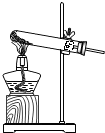 加热液体 | ||
| C. | 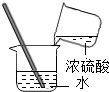 稀释浓硫酸 | D. | 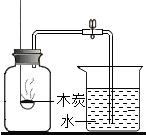 测定空气中氧气的含量 |
 A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如下图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件已略去)
A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如下图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件已略去)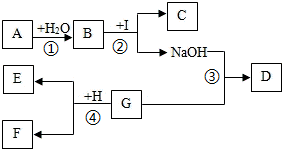 如图所示,A~I为初中化学学习中常见的物质,其中A是生活中一种常见的干燥剂,C是石灰石的主要成分,G是一种蓝色溶液,E是一种红色固体,“→”表示物质间存在着相互转化关系(部分生成物未标出).请回答下列问题.
如图所示,A~I为初中化学学习中常见的物质,其中A是生活中一种常见的干燥剂,C是石灰石的主要成分,G是一种蓝色溶液,E是一种红色固体,“→”表示物质间存在着相互转化关系(部分生成物未标出).请回答下列问题.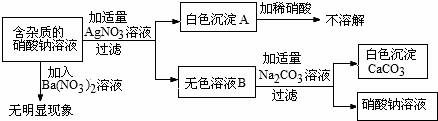
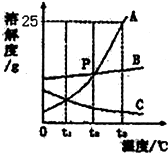 如图是A、B、C三种物质的溶解度曲线.
如图是A、B、C三种物质的溶解度曲线.