题目内容
15.向硫酸铜溶液中加入一定量的镁粉,完全反应后过滤,得滤渣和蓝色滤液,下列说法正确的是( )| A. | 滤渣中一定有铜,可能有镁 | B. | 滤液中只有硫酸镁 | ||
| C. | 向滤渣中滴加稀盐酸,无气泡产生 | D. | 滤液中只有硫酸铜 |
分析 镁的金属活动性比铜强,向硫酸铜溶液中加入一定量的镁粉,生成硫酸镁溶液和铜,完全反应后过滤,得滤渣和蓝色滤液,得到蓝色滤液,说明硫酸铜溶液有剩余,据此进行分析判断.
解答 解:镁的金属活动性比铜强,向硫酸铜溶液中加入一定量的镁粉,生成硫酸镁溶液和铜,完全反应后过滤,得滤渣和蓝色滤液,说明硫酸铜溶液有剩余.
A、镁与硫酸铜溶液反应生成硫酸镁溶液和铜,硫酸铜溶液有剩余,滤渣中一定有铜,不可能有镁,故选项说法错误.
B、镁与硫酸铜溶液反应生成硫酸镁溶液和铜,硫酸铜溶液有剩余,滤液中含有硫酸镁、硫酸铜,故选项说法错误.
C、镁与硫酸铜溶液反应生成硫酸镁溶液和铜,硫酸铜溶液有剩余,滤渣是铜,铜与稀盐酸不反应,向滤渣中滴加稀盐酸,无气泡产生,故选项说法正确.
D、镁与硫酸铜溶液反应生成硫酸镁溶液和铜,硫酸铜溶液有剩余,滤液中含有硫酸镁、硫酸铜,故选项说法错误.
故选:C.
点评 本题难度不大,熟练掌握金属的化学性质、根据蓝色滤液确定硫酸铜溶液有剩余是正确解答本题的关键.

练习册系列答案
 冲刺100分1号卷系列答案
冲刺100分1号卷系列答案
相关题目
5.下列物质之间的转化,经过一步反应不能实现的是( )
| A. | Cu→Cu(NO3)2 | B. | Fe2O3→FeCI2 | C. | CH4→H2O | D. | H2SO4→HCI |
3.下列实验操作错误的是( )
| A. | 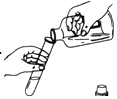 倾倒液体 | B. | 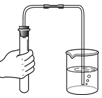 检查装置的气密性 | ||
| C. | 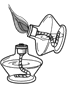 点燃酒精灯 | D. | 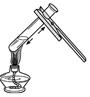 加热试管中液体 |
10.下列生活用品所使用的主要材料属于有机合成材料的是( )
| A. | 纯棉围巾 | B. | 塑料保鲜膜 | C. | 不锈钢剪刀 | D. | 陶瓷碗 |
4.分离、提纯是化学实验的重要环节,下列实验设计不能达到实验目的是( )
| 实验目的 | 实验设计 | |
| A | 除去FeSO4溶液中的CuSO4 | 先加入足量的铁粉,再过滤 |
| B | 除去NaCl固体中的少量Na2CO3 | 先加足量水溶解,再加适量稀盐酸,蒸发结晶 |
| C | 除去KNO3溶液中的少量K2SO4 | 加入适量的BaCl2溶液,过滤 |
| D | 除去铜粉中混有的少量铁粉 | 用磁铁吸引 |
| A. | A | B. | B | C. | C | D. | D |
 )与B(
)与B(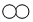 )反应生成C(
)反应生成C( ),如图是其反应前后分子及其数目变化的微观示意图
),如图是其反应前后分子及其数目变化的微观示意图 和
和 表示两种质子数不同的原子)
表示两种质子数不同的原子)