题目内容
2.2015年中国科学家屠呦呦因青蒿素(C15H22O5)和双氢青蒿素(C15H24O5)而荣获了诺贝尔奖.下列有关说法中不正确的是( )| A. | 青蒿素比双氢青蒿素少两个氢原子 | |
| B. | 青蒿素和双氢青蒿素都属于有机物 | |
| C. | 青蒿素和双氢青蒿素中碳、氧原子个数比都为3:1 | |
| D. | 青蒿素氧元素的质量分数比双氢青蒿素中氧元素的质量分数大 |
分析 A.根据分子结构来分析;
B.根据有机物的定义来分析;
C.根据分子结构来分析;
D.根据元素的质量分数计算方法来分析
解答 解:A.一个双氢青蒿素分子比一个青蒿素分子多两个氢原子,故错误;
B.由二者的化学式可知,二者都属于有机物,故正确;
C.由青蒿素(C15H22O5)和双氢青蒿素(C15H24O5)化学式可知,二者分子中碳、氧原子个数比都为3:1;故正确;
D.青蒿素中氧元素的质量分数=$\frac{16×5}{12×15+1×22+16×5}$,双氢青蒿素中氧元素的质量分数=$\frac{16×5}{12×15+1×24+16×5}$,可见说法正确.
故选A
点评 本题主要考查化学式的意义、根据化学式确定组成物质元素之间的质量关系、及相对分子质量计算方法的掌握,进行解题的能力.

练习册系列答案
相关题目
12.如图是X、Y、Z三种液体的对应近似pH,下列判断不正确的是( )
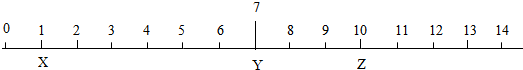
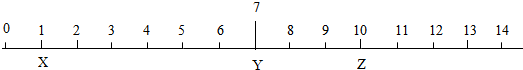
| A. | X显酸性 | B. | Y一定是水 | ||
| C. | Z可能是碳酸钠溶液 | D. | Z可使紫色石蕊试液变蓝 |
10.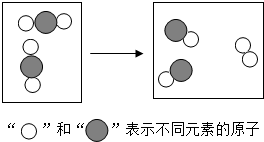 某反应前后分子变化的微观示意图如下,下列说法正确的是( )
某反应前后分子变化的微观示意图如下,下列说法正确的是( )
 某反应前后分子变化的微观示意图如下,下列说法正确的是( )
某反应前后分子变化的微观示意图如下,下列说法正确的是( )| A. | 反应物与生成物共有5种物质 | B. | 反应后原子的个数增多 | ||
| C. | 该图可示意SO2与O2的反应 | D. | 该反应属于分解反应 |
17.下列变化中,属于化学变化的是( )
| A. | 干冰升华 | B. | 纸张燃烧 | C. | 铜丝折弯 | D. | 酒精挥发 |
7.除去下列物质中混有的少量杂质(括号内为杂质),拟定的实验方案不可行的是( )
| A. | NaCl溶液(MgCl2)-加入过量的NaOH溶液,过滤,滤液中加稀盐酸至中性 | |
| B. | 氧气(水蒸气)-通过装有足量无水氯化钙的干燥管 | |
| C. | CaO固体(CaCO3)-高温充分煅烧 | |
| D. | 氢气(氯化氢气体)-依次通过足量的NaHCO3溶液和浓硫酸 |
14.下列变化属于化学变化的是( )
| A. | 蜡烛熔化 | B. | 铁水铸锅 | C. | 纸张燃烧 | D. | 海水晒盐 |
18. 在今天的化学兴趣小组活动中,指导老师拿来了一包已经失效的石灰干燥剂.为了确定该干燥剂的组成,同学们进行了如下的探究活动:
在今天的化学兴趣小组活动中,指导老师拿来了一包已经失效的石灰干燥剂.为了确定该干燥剂的组成,同学们进行了如下的探究活动:
小萌同学通过探究发现,此包装袋中的生石灰干燥剂已经完全变质失效.他采用的探究方法是:取少量样品于试管中,加入少量水,用手触摸试管外壁,没有明显的放热现象.此实验中加入的水必须是少量的,理由是如果所加的水较多,则水会吸收反应产生的热量,影响实验的结论.
【查阅资料】
石灰干燥剂的成分为CaO,请写出该干燥剂干燥原理CaO+H2O=Ca(OH)2(用化学方程式表示).
【提出猜想】①该干燥剂的成分为Ca(OH)2
②该干燥剂的成分为CaCO3
③你的猜想是CaCO3、Ca(OH)2;
【方案设计】小组成员设计了如下的实验方案:
方案一:取样滴加稀盐酸,有气泡产生,则白色固体只存在CaCO3;
方案二:取样滴加少量稀盐酸,没有气泡产生,则白色固体中只存在Ca(OH)2;
方案三:取样加入水中,振荡,静置,上层为清液,下层出现固体不溶物,取上层清液滴加酚酞试液,变红,则固体为CaCO3和Ca(OH)2的混合物.
【实验分析】小组成员经过讨论发现上述实验方案都存在着问题.
(1)上述方案一中存在的问题是不能说明白色固体中是否含有Ca(OH)2.
(2)上述方案二的结论是错误的,原因是由于加入的盐酸是少量的,可能只是与氢氧化钙发生了反应,还没有与碳酸钙反应,无法证明没有碳酸钙的存在.
(3)实验方案三中的结论也有些不妥,是因为不能说明白色固体中含有CaCO3,因为不溶物可能是微溶于水的氢氧化钙.
(4)实验证实,该固体是CaCO3和Ca(OH)2的混合物,请你再设计一种实验方案予以证明,只要写出实验步骤和现象即可.
【数据分析】
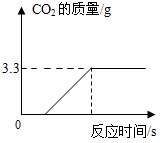
为了进一步确定该混合物中CaCO3的质量分数,实验小组的同学取了15克样品,加入足量的稀盐酸,实验测得生成CO2气体的质量如图所示,请据图计算该混合物中CaCO3的质量分数.
【反思与评价】
实验中造成计算结果与实际值相比偏小,则可能的原因是有部分生成的二氧化碳气体因溶解于水而没有全部逸出.
 在今天的化学兴趣小组活动中,指导老师拿来了一包已经失效的石灰干燥剂.为了确定该干燥剂的组成,同学们进行了如下的探究活动:
在今天的化学兴趣小组活动中,指导老师拿来了一包已经失效的石灰干燥剂.为了确定该干燥剂的组成,同学们进行了如下的探究活动:小萌同学通过探究发现,此包装袋中的生石灰干燥剂已经完全变质失效.他采用的探究方法是:取少量样品于试管中,加入少量水,用手触摸试管外壁,没有明显的放热现象.此实验中加入的水必须是少量的,理由是如果所加的水较多,则水会吸收反应产生的热量,影响实验的结论.
【查阅资料】
石灰干燥剂的成分为CaO,请写出该干燥剂干燥原理CaO+H2O=Ca(OH)2(用化学方程式表示).
【提出猜想】①该干燥剂的成分为Ca(OH)2
②该干燥剂的成分为CaCO3
③你的猜想是CaCO3、Ca(OH)2;
【方案设计】小组成员设计了如下的实验方案:
方案一:取样滴加稀盐酸,有气泡产生,则白色固体只存在CaCO3;
方案二:取样滴加少量稀盐酸,没有气泡产生,则白色固体中只存在Ca(OH)2;
方案三:取样加入水中,振荡,静置,上层为清液,下层出现固体不溶物,取上层清液滴加酚酞试液,变红,则固体为CaCO3和Ca(OH)2的混合物.
【实验分析】小组成员经过讨论发现上述实验方案都存在着问题.
(1)上述方案一中存在的问题是不能说明白色固体中是否含有Ca(OH)2.
(2)上述方案二的结论是错误的,原因是由于加入的盐酸是少量的,可能只是与氢氧化钙发生了反应,还没有与碳酸钙反应,无法证明没有碳酸钙的存在.
(3)实验方案三中的结论也有些不妥,是因为不能说明白色固体中含有CaCO3,因为不溶物可能是微溶于水的氢氧化钙.
(4)实验证实,该固体是CaCO3和Ca(OH)2的混合物,请你再设计一种实验方案予以证明,只要写出实验步骤和现象即可.
| 实验操作步骤 | 实验现象 |
| (1)取样,滴加足量稀盐酸 (2)另取适量的样品,加足量的水溶解,静置取上层清液,滴加酚酞试液 | (1)产生大量的气泡 (2)溶液呈红色 |
为了进一步确定该混合物中CaCO3的质量分数,实验小组的同学取了15克样品,加入足量的稀盐酸,实验测得生成CO2气体的质量如图所示,请据图计算该混合物中CaCO3的质量分数.
【反思与评价】
实验中造成计算结果与实际值相比偏小,则可能的原因是有部分生成的二氧化碳气体因溶解于水而没有全部逸出.