题目内容
1.为测得某大理石样品中碳酸钙的质量分数,兴趣小组同学进行了如下实验,过程如图所示:(杂质不溶于水也不与盐酸反应)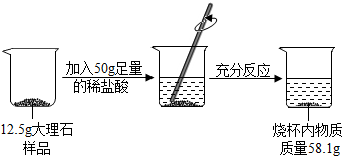
求:①反应中生成二氧化碳的质量为4.4g;
②该大理石样品中碳酸钙的质量分数.
分析 ①根据质量守恒定律,反应前后减少的质量为二氧化碳的质量.
②利用碳酸钙与盐酸反应的化学方程式,根据二氧化碳的质量可求出碳酸钙的质量,即可求出大理石中碳酸钙的质量分数.
解答 解:①根据质量守恒定律,产生CO2的质量的为:12.5g+50g-58.1g=4.4g;故填:4.4g;
②设大理石样品中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{x}=\frac{44}{4.4g}$
x=10g
大理石样品中碳酸钙的质量分数为:$\frac{10g}{12.5g}$×100%=80%
答:大理石样品中碳酸钙的质量分数为80%.
点评 根据化学方程式进行计算时,只能使用纯净物的质量进行计算,而不能把混合物的质量直接代入化学方程式进行计算,有关反应前后质量减少的计算是初中化学计算的一个常见内容,一般的规律是依据质量的变化求出某一生成的质量.

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目
11.下列物质的检验与除去杂质实验叙述中,错误的是( )
| A. | 除去NaHCO3溶液中混有的Na2CO3,可以通入适量的二氧化碳 | |
| B. | 除去BaCl2溶液中的少量HCl,可以加入过量的BaCO3,然后过滤 | |
| C. | 某溶液中滴加稀盐酸,有气泡生成,将气体通入澄清石灰水变浑浊,该溶液中一定是碳酸根离子 | |
| D. | 在久置的某氢氧化钠溶液中滴加酚酞,溶液变红;再加入过量的氯化钡溶液,有白色沉淀生成,同时溶液变为无色.说明该氢氧化钠溶液已经部分变质 |
13.用盐酸和酚酞混合液浸过的滤纸,若在滤纸上分别滴入下列溶液,滤纸上不会出现红色的是( )
| A. | 氯化钠溶液 | B. | 稀硫酸 | C. | 石灰水 | D. | 氢氧化钠 |
10.下列物质的归类正确的是( )
| A. | 同一物质:火碱,纯碱,苛性钠 | B. | 复合肥料:氯化铵、磷矿粉、硝酸钾 | ||
| C. | 化石燃料:煤、石油、天然气 | D. | 混合物:氢气、石灰石、空气 |
 某班同学合作制作了如图所示的简易电解水装置.根据实验回答下列问题:
某班同学合作制作了如图所示的简易电解水装置.根据实验回答下列问题: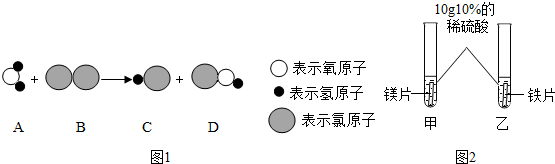
 别拿土豆不当粮食,据报道:我国即将启动“马铃薯(即土豆)主粮化”战略,推进把马铃薯做为第四大主粮.今后把土豆加工成馒头、面包、面条等做为餐桌上的主食,如图是土豆种植.试回答:
别拿土豆不当粮食,据报道:我国即将启动“马铃薯(即土豆)主粮化”战略,推进把马铃薯做为第四大主粮.今后把土豆加工成馒头、面包、面条等做为餐桌上的主食,如图是土豆种植.试回答: