题目内容
19.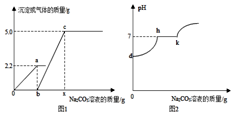 小科同学在实验室制取CO2气体后,对废液进 行探究,他向一定质量的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液质量与产生沉淀或气体的质量关系如图1所示:加入Na2CO3溶液的质量与溶液的pH变化关系如图2所示,请写出h-k段的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl,a点溶液中所含溶质为NaCl和CaCl2(用化学式表示).
小科同学在实验室制取CO2气体后,对废液进 行探究,他向一定质量的含CaCl2和HCl的废液中逐滴加入溶质质量分数为10%的Na2CO3溶液.实验过程中加入Na2CO3溶液质量与产生沉淀或气体的质量关系如图1所示:加入Na2CO3溶液的质量与溶液的pH变化关系如图2所示,请写出h-k段的化学方程式Na2CO3+CaCl2=CaCO3↓+2NaCl,a点溶液中所含溶质为NaCl和CaCl2(用化学式表示).
分析 根据碳酸钠和盐酸反应生成氯化钠、水和二氧化碳气体,溶液的pH值上升,然后碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,溶液的pH值不变,然后随着碳酸钠的滴加,溶液的pH值逐渐增大进行分析.
解答 解:碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,有气体生成,溶液的pH值上升,分别表示图1中的o-a段和图2中的d-h段;然后碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,溶液的pH值不变,分别表示图1中的b-c段和图2中的h-k段;然后随着碳酸钠的滴加,溶液的pH值逐渐增大,所以h-k段的化学方程式为Na2CO3+CaCl2=CaCO3↓+2NaCl,a点表示碳酸钠先盐酸反应,把盐酸消耗完,故溶液中的溶质为氯化钠和氯化钙;.
故答案为:Na2CO3+CaCl2=CaCO3↓+2NaCl;NaCl和CaCl2.
点评 解答本题关键要知道只有把盐酸反应完了,才能与氯化钙反应产生沉淀,因为如果碳酸钠与氯化钙先反应生成了碳酸钙沉淀,也会被剩余的盐酸溶解掉,将不会看到沉淀.

练习册系列答案
 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案
相关题目
9.小明发现植物出现叶片发黄、茎秆倒伏现象,急需施加复合肥,下列化肥符合要求的是( )
| A. | KCl | B. | Ca(H2PO4)2 | C. | (NH4)2SO4 | D. | KNO3 |
4.经实验测得某一溶液由Na+、Mg2+、Cl-、SO42-四种离子组成,其中含有4.6gNa+、14.4克SO42-、14.2克Cl-,则Mg2+的质量为( )
| A. | 2.4克 | B. | 5克 | C. | 6克 | D. | 4.8克 |
9.制造下列物品所用的主要材料,不需要通过化学反应就能得到的是( )
| A. | 青铜剑 | B. | 大理石雕塑 | C. | 合成橡胶轮胎 | D. | 高强度降落伞 |