题目内容
2.有限的元素可组成种类繁多的物质.依据表中的元素回答下列问题.| 元素名称 | 氢 | 碳 | 氧 | 氯 | 锰 | 铁 |
| 元素符号 | H | C | O | Cl | Mn | Fe |
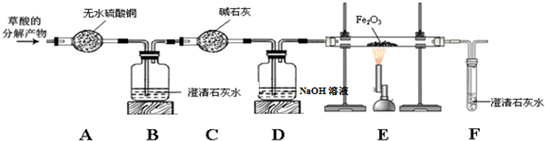
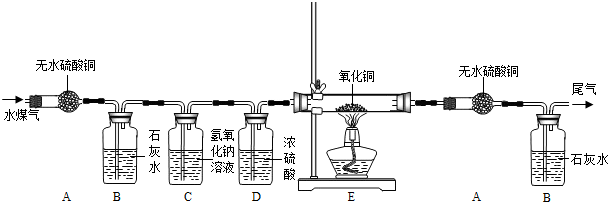
(2)气体单质E与红色固体F在一定条件下反应,得到固体G,反应的化学方程式为3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+2H2O.
(3)将一定量的固体G放入过量M溶液中,能发生反应,观察到的现象是有气泡产生,溶液由无色变成浅绿色.
(4)向(3)所得溶液中加入适量A溶液,溶液变为黄色,且溶质仅有一种,该反应的化学方程式为2FeCl2+2HCl+H2O2=2FeCl3+2H2O.
分析 根据A溶液在黑色固体B的作用下生成无色气体D,D与生命活动息息相关,所以D是氧气,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,所以A是过氧化氢溶液,B是二氧化锰,气体单质E与红色固体F在一定条件下反应,得到固体G,所以F是氧化铁,氢气和氧化铁反应生成铁和水,所以G是铁,将一定量的铁放入过量M溶液中,能发生反应,所以M是稀盐酸,铁和盐酸反应生成氯化亚铁和氢气,向(3)所得溶液中加入适量过氧化氢溶液,溶液变为黄色,且溶质仅有一种,过氧化氢将氯化亚铁氧化成氯化铁,然后将推出的物质进行验证即可.
解答 解:A溶液在黑色固体B的作用下生成无色气体D,D与生命活动息息相关,所以D是氧气,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,所以A是过氧化氢溶液,B是二氧化锰,气体单质E与红色固体F在一定条件下反应,得到固体G,所以F是氧化铁,氢气和氧化铁反应生成铁和水,所以G是铁,将一定量的铁放入过量M溶液中,能发生反应,所以M是稀盐酸,铁和盐酸反应生成氯化亚铁和氢气,向(3)所得溶液中加入适量过氧化氢溶液,溶液变为黄色,且溶质仅有一种,过氧化氢将氯化亚铁氧化成氯化铁,经过验证,推导正确,所以
(2)氢气和氧化铁在高温的条件下反应生成铁和水,化学方程式为:3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+2H2O;
(3)铁和盐酸反应生成氯化亚铁和氢气,观察到的现象是:有气泡产生,溶液由无色变成浅绿色;
(4)过氧化氢溶液和氯化亚铁反应生成氯化铁和水,化学方程式为:2FeCl2+2HCl+H2O2=2FeCl3+2H2O.
故答案为:(1)3H2+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+2H2O;
(3)有气泡产生,溶液由无色变成浅绿色;
(4)2FeCl2+2HCl+H2O2=2FeCl3+2H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | 氯化镁 | B. | 氩气 | C. | 高锰酸钾 | D. | 氨气 |
(1)糖类、油脂、蛋白质和维生素都是人类的基本营养物质.下表为某品牌燕麦片标签中的一部分.
| 每100g含有 营养成分 | 糖类 | 油脂 | 蛋白质 | 维生素C | 钙 | 镁 | 钠 | 锌 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 18.2mg | 30.8mg | 8.1mg |
②维生素C易溶于水,向其水溶液中滴入紫色石蕊试液,石蕊变红色,加热该溶液至沸腾,红色消失.因此,烹调富含维生素C的食物时,应该注意不要高温加热;在碱性条件下,维生素C易被空气氧化,烧煮时最好加一点食醋.
| A. | 该塑料不属于有机合成材料 | B. | 有助于减少“白色污染” | ||
| C. | 有助于减缓“温室效应” | D. | 是纳米技术应用的重要突破 |
| A. | 钢铁 | B. | 金刚石 | C. | 塑料 | D. | 玻璃 |
 水是生命之源,爱护水资源是每个公民应尽的责任.请回答下列有关问题:
水是生命之源,爱护水资源是每个公民应尽的责任.请回答下列有关问题: