题目内容
9.“见著知微,见微知著”是重要的化学思维方法.课堂上,老师给出了A、B、C、D四种粒子的结构示意图(如图所示),同学们畅所欲言,纷纷发表了自己的看法.请回答下列问题:
(1)从宏观知微观.
①50mL水与50mL乙醇混合后,溶液体积小于100mL,微观解释为分子间有间隔;
②同学们都喜欢将洗过的衣服放在太阳底下晾晒,微观解释为温度高,分子运动速度快;
(2)从微观知宏观.
①微粒A最外层电子数是1,在化学反应中容易失(填“得”或“失”)电子.
②丙同学的观点不正确,其理由是D粒子的质子数大于核外电子数,是阳离子.
③微粒A与微粒C形成的化合物的名称为硫化钠;化学式为Na2S.
分析 (1)①根据分子之间有间隔的特性分析解答,②根据温度高、分子运动速度快分析回答;
(2)①根据原子结构示意图的意义、元素的性质与原子结构的关系分析回答;
②根据质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子分析回答;
③根据原子的最外层电子数可判断得失电子情况、并判断元素的化合价,书写物质的化学式.
解答 解:(1)①由于分子之间有间隔,50mL水与50mL乙醇混合后,分子相互占据了间隔,所以混合后溶液体积小于100mL;
②同学们都喜欢将洗过的衣服放在太阳底下晾晒,是由于温度高,水分子运动速度快,所以干的更快;
(2)①由原子结构示意图可知,微粒A最外层电子数是1,小于4,在化学反应中容易失去电子;
②微粒A、B、C、D中,D粒子的质子数是11,核外电子数是10,质子数大于核外电子数,是阳离子,所以丙同学的观点不对;
③微粒A是11号元素--钠元素,最外层电子数是1,易失去1个电子达到稳定结构,化合价是+1价,微粒C是16号元素,最外层电子数是6,易得2个电子达到稳定结构,化合价是-2价,二者形成的化合物的化学式是:Na2S,读法:由后向前读作:硫化钠;
故答案为:(1)①分子间有间隔 ②温度高,分子运动速度快;
(2)①1; 失; ②丙;D粒子的质子数大于核外电子数,是阳离子;③硫化钠;Na2S.
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
3.下列各组中的物质,在溶液中不能发生反应的是( )
| A. | Ba(OH)2和K2CO3 | B. | 稀HCl和Na2CO3 | C. | KNO3和NaCl | D. | Fe(OH)3和HNO3 |
4.工业铁红的主要成分是Fe2O3,还含有少量的FeO、Fe3O4.
为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析.
【资料1】草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4•3H2O$→_{△}^{浓H_{2}SO_{4}}$ CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是d(填字母编号).

【问题讨论】用图所示装置进行实验:
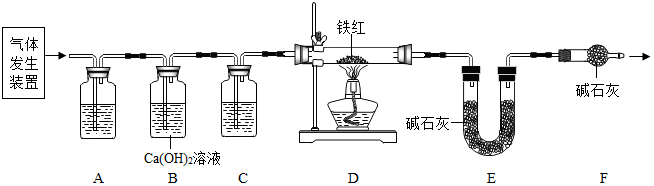
(2)实验前应先检查装置气密性.
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是c、a(填字母编号).
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是检验二氧化碳是否被氢氧化钠溶液完全吸收.
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前排出装置中的空气,避免发生安全事故. ②停止加热后使反应生成的二氧化碳全部被碱石灰吸收.
(6)写出D装置中所发生反应的一个化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,或FeO+CO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2,或Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
【数据分析与计算】【资料2】铁的常见氧化物中铁的质量分数:
(7)称取铁红样品10.0g,用上述装置进行实验,测定铁红中铁的质量分数.
①D中充分反应后得到Fe粉的质量为m g,则14.0<m<15.56.
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是76%.
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会偏小(填“偏小”、“不变”或“偏大”).
反思2:请指出【问题讨论】中实验装置的一个明显缺陷没有处理尾气 .
为了测定铁红中铁的质量分数,兴趣小组的同学进行了如下实验,请你参与过程分析.
【资料1】草酸晶体(H2C2O4•3H2O)在浓H2SO4作用下受热分解,化学方程式为:
H2C2O4•3H2O$→_{△}^{浓H_{2}SO_{4}}$ CO2↑+CO↑+4H2O
(1)下列可用作草酸分解制取气体的装置是d(填字母编号).

【问题讨论】用图所示装置进行实验:

(2)实验前应先检查装置气密性.
(3)进入D中的气体是纯净、干燥的CO,则A、C中的试剂依次是c、a(填字母编号).
a.浓硫酸 b.澄清的石灰水 c.氢氧化钠溶液
(4)B装置的作用是检验二氧化碳是否被氢氧化钠溶液完全吸收.
(5)对D装置加热前和停止加热后,都要通入过量的CO,其作用分别是:
①加热前排出装置中的空气,避免发生安全事故. ②停止加热后使反应生成的二氧化碳全部被碱石灰吸收.
(6)写出D装置中所发生反应的一个化学方程式Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,或FeO+CO$\frac{\underline{\;高温\;}}{\;}$Fe+CO2,或Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2.
【数据分析与计算】【资料2】铁的常见氧化物中铁的质量分数:
| 铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
| 铁的质量分数 | 77.8% | 70.0% | 72.4% |
①D中充分反应后得到Fe粉的质量为m g,则14.0<m<15.56.
②实验前后称得E装置增重6.6g,则此铁红中铁的质量分数是76%.
【实验评价】
反思1:本实验中如果缺少C装置(不考虑其它因素),则测得样品中铁的质量分数会偏小(填“偏小”、“不变”或“偏大”).
反思2:请指出【问题讨论】中实验装置的一个明显缺陷没有处理尾气 .
14.西藏地区独特的高原风景早就吸引了丫丫,她很想在国庆期间前往观光.但爸爸说初到西藏时会发生不同程度的“高原反应”,这是由于( )
| A. | 高原地区的氧气与平原地区的氧气的化学性质不同 | |
| B. | 高原地区空气中氧气含量过高,让人有压抑感 | |
| C. | 高原地区空气中二氧化碳含量过高让人感到窒息 | |
| D. | 高原地区空气稀薄,氧气的体积分数仍为2l%、 |
1.下列措施或事故处理方法正确的是( )
| A. | 电器着火时立即用水扑灭 | |
| B. | 天然气泄漏时,立即打开排气扇电源开关 | |
| C. | 用湿毛巾捂住口鼻低下身子逃出火场 | |
| D. | 酒精泼洒桌面燃烧,迅速用水浇灭 |
 如图所示,集气瓶中分别进行硫粉和铁丝在氧气中燃烧的实验.请回答:
如图所示,集气瓶中分别进行硫粉和铁丝在氧气中燃烧的实验.请回答: