题目内容
4.肥田粉的主要成分是硫酸铵.现有一包标有含氮量为20.0%的肥田粉样品,甲、乙两同学为了计算该肥田粉中硫酸铵的质量分数,他们各称取7.5g样品,分别采用下列方法:甲同学根据化学式计算:
解:硫酸铵中氮元素的质量分数:$\frac{N的相对原子质量}{(NH4)2SO4的相对分子质量}$×100%=$\frac{14×2}{132}$×100%=21.2%
设7.5g样品中硫酸铵的质量为x. x×21.2=7.5g×20.0% x=7.08g
样品中硫酸铵的质量分数为:$\frac{7.08g}{7.5g}$×100%=94.4%
答:样品中硫酸铵的质量分数为94.4%
乙同学通过实验方法并根据化学方程式计算:
将称取的7.5g样品与足量的熟石灰混合加热,直至不再产生气体为止,得到纯净、干燥的氨气1.7g.该反应的化学方程式为:(NH4)2SO4+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaSO4+2NH3↑+2H2O
(乙同学下面的计算过程由你帮助完成)
(1)请你根据乙同学的实验结果,计算样品中硫酸铵的质量分数.(计算结果精确至0.1% )
(2)你的计算结果和甲同学的计算结果不同的原因是计算依据不同:甲同学默认的是标注的含氮量20.0%是准确的;乙的计算不考虑标注,而是以实验为依据.
分析 (1)根据生成的氨气的质量和对应的化学方程式求算硫酸铵的质量,进而求算其质量分数;
(2)由于甲同学计算时默认的“标有含氮量为20.0%“是准确的,所以计算结果就和乙不一致.乙的计算不考虑标准,而是以实验为依据.
解答 解:(1)设硫酸铵的质量为x
(NH4)2SO4+Ca(OH)2 $\frac{\underline{\;\;△\;\;}}{\;}$CaSO4+2NH3↑+2H2O
132 34
x 1.7g
$\frac{132}{34}$=$\frac{x}{1.7g}$
x=6.6g
样品中硫酸铵的质量分数为$\frac{6.6g}{7.5g}$×100%=88.0%
(2)计算依据不同:甲同学默认的是标注的含氮量20.0%是准确的;乙的计算不考虑标注,而是以实验为依据,所以导致结果不同.
答:(1)样品中硫酸铵的质量分数为88.0%.
(2)你的计算结果和甲同学的计算结果不同的原因是 计算依据不同:甲同学默认的是标注的含氮量20.0%是准确的;乙的计算不考虑标注,而是以实验为依据.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
14.下列关于化学变化的说法不正确的是( )
| A. | 化学反应往往伴随着能量的变化.通常表现为热量的变化 | |
| B. | 化学反应前后,催化剂的质量和性质都不变 | |
| C. | 化学反应前后,元素的种类和原子的个数都不变 | |
| D. | 化学反应前后,物质的种类和分子的种类都会变 |
19.去年春季,我国西南地区发生了一场特大旱灾,国家投入大量人力物力来保障灾区人民的基本生活用水.下列关于水的认识正确的是( )
| A. | 水是良好的溶剂,许多物质都能溶于水 | |
| B. | 地球上各种水体之间是互不联系的 | |
| C. | 为了节约用水,提倡用危害性小的工业废水直接灌溉农田 | |
| D. | 用沉淀法、过滤法和蒸馏法净化水,效果最好的是过滤法 |
16.下列常见材料中属于有机合成材料的是( )
| A. | 大理石 | B. | 不锈钢 | C. | 生铁 | D. | 塑料 |
13.如图是某化学反应的微观模拟示意图,下列说法正确的是( )
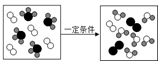

| A. | 该反应属于置换反应 | B. | 反应前后原子种类不变、数目改变 | ||
| C. | 反应物中包含两种化合物 | D. | 发生反应的分子个数比为 1:1 |

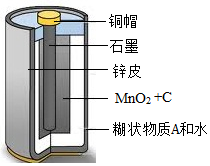 化学电池是一类重要的能源,按工作性质可分为:一次电池(例如干电池)和二次电池(可充电电池,例如铅酸蓄电池).请简要回答下列各空
化学电池是一类重要的能源,按工作性质可分为:一次电池(例如干电池)和二次电池(可充电电池,例如铅酸蓄电池).请简要回答下列各空 小明和同学到野外郊游,请根据题目给出的信息填空.
小明和同学到野外郊游,请根据题目给出的信息填空.