题目内容
1.已知 、
、 、
、 分别表示X、Y、Z三种不同的气体分子,在一定条件下的变化如图所示,由图示获得的下列信息中正确的是C.
分别表示X、Y、Z三种不同的气体分子,在一定条件下的变化如图所示,由图示获得的下列信息中正确的是C.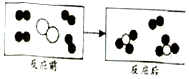
A、该反应不符合质量守恒定律 B、
 可能是一氧化碳
可能是一氧化碳C、在化学变化中,分子一定发生改变 D、该反应的化学方程式可表示为3X+Y=2Z(用X、Y、Z分别表示反应物、生成物、反应条件忽略)
分析 已知 、
、 、
、 分别表示X、Y、Z三种不同的气体分子的模型看出,X、Y属于单质,Z属于化合物,比较反应前后的图形,发现三个X和一个Y反应,生成了两个Z,有一个X分子没有参加反应,据此分析解答;
分别表示X、Y、Z三种不同的气体分子的模型看出,X、Y属于单质,Z属于化合物,比较反应前后的图形,发现三个X和一个Y反应,生成了两个Z,有一个X分子没有参加反应,据此分析解答;
解答 解:根据参加反应的分子数和生成的分子数可知该反应的图示可表示为
A、该反应符合质量守恒定律,此说法错误;
B、 不可能是一氧化碳,为单质,故此项说法错误;
不可能是一氧化碳,为单质,故此项说法错误;
C、在化学变化中,分子一定发生改变,此说法正确;
故选C.
补充D、该反应的化学方程式可表示为3X+Y=2Z.
点评 认真阅读分子模型和反应的模拟图结合化学变化的实质及分子、原子之间的关系,能判断分子的构成和物质的分类,是解决这类题目的关键点.

练习册系列答案
相关题目
12.下表是NaCl、KClO3在不同温度下的溶解度(单位:g/100g水).
(1)20℃时,NaCl的溶解度为36.0g;40℃时,将20g KClO3放入100g水中,所得溶液溶质质量分数为12.2%(精确到0.1%).
(2)“海水晒盐”利用的方法是蒸发结晶(填“蒸发结晶”或“降温结晶”);
(3)工业上用氯化钠溶液制备氯酸钾,主要流程如下:

①上述流程中,氯化钠溶液中的水是否参与第I步化学反应?是(填“是”或“否”),你的判断依据是元素守恒.
②写出第III步中发生反应的化学方程式NaClO3+KCl=NaCl+KClO3.
③溶液A中的溶质除NaCl外,还含有KCl、KClO3(填化学式).
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| S(NaCl) | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| S(KClO3) | 3.3 | 7.3 | 13.9 | 23.8 | 37.5 | 56.3 |
(2)“海水晒盐”利用的方法是蒸发结晶(填“蒸发结晶”或“降温结晶”);
(3)工业上用氯化钠溶液制备氯酸钾,主要流程如下:

①上述流程中,氯化钠溶液中的水是否参与第I步化学反应?是(填“是”或“否”),你的判断依据是元素守恒.
②写出第III步中发生反应的化学方程式NaClO3+KCl=NaCl+KClO3.
③溶液A中的溶质除NaCl外,还含有KCl、KClO3(填化学式).
16.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是( )
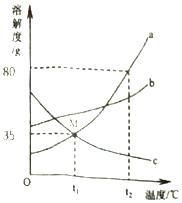

| A. | M点表示a、c两种物质的饱和溶液质量相等 | |
| B. | t1℃时,b物质的饱和溶液升温至t2℃时仍是饱和溶液 | |
| C. | 将t1℃时三种物质的饱和溶液升温到t2℃时,所得溶液中溶质的质量分数的大小关系是:b>a=c | |
| D. | t1℃时,a物质的饱和溶液中溶质和溶剂的质量比为7:20 |
6.某校化学兴趣小组的同学测定了来自三个不同地方的铜和硫的化合物样品,实验数据如下:
根据表中数据,你能得出的结论是( )
| 样品 | 样品质量/g | 铜元素的质量/g | 硫元素的质量/g |
| 1 | 5.02 | 3.35 | 1.67 |
| 2 | 10.05 | 6.71 | 3.34 |
| 3 | 99.6 | 66.4 | 33.2 |
| A. | 样品1中铜元素的质量分数为50% | |
| B. | 样品2的化合物的化学式是Cu2S | |
| C. | 样品3中铜元素与硫元素的质量比为2:1 | |
| D. | 三个不同地方样品可能属于同一种物质 |
13.雾霾已经成为2017年全国两会上反映较为突出的环境问题.李克强总理作出重要指示,攻克北方雾霾的形成机理,让广大人民群众看到更多的蓝天.下列有关环境保护问题的叙述中,不正确的是( )
| A. | “绿色化学”是指对环境无负面影响的化学 | |
| B. | “白色污染”主要是指白色粉尘对环境造成的污染 | |
| C. | “温室气体”主要是指CO2和CH4等气体 | |
| D. | “酸雨”是由大气中含有硫和氮的氧化物等导致的 |
10.不能达到实验目的方案是( )
| A. | 用稀硫酸鉴别炭粉和氧化铜 | |
| B. | 用锌粒鉴别食盐水和稀盐酸 | |
| C. | 用硝酸银溶液鉴别稀盐酸和稀硫酸 | |
| D. | 用燃着的木条鉴别氢气、氧气和二氧化碳 |
11. 石灰石是主要修路材料之一,某兴趣小组用修路材料石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,该小组取石灰石20g,将一定质量的稀盐酸平均分5次加入其中,记录数据如下:
石灰石是主要修路材料之一,某兴趣小组用修路材料石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,该小组取石灰石20g,将一定质量的稀盐酸平均分5次加入其中,记录数据如下:
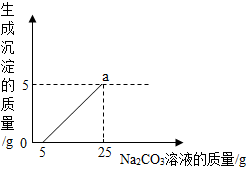
在准备将反应后的废液倒进废液缸时,发现实验桌上有一拼未知质量分数的Na2CO3溶液,他们决定利用该废液,测定这瓶Na2CO3溶液中溶质的质量分数.他们将废液过滤,取部分溶液的质量与生产沉淀质量的关系如图所示.请计算:
(1)表中m=13.4;
(2)当20g石灰石完全反应时生成CO2的质量;
(3)Na2CO3溶液中溶质的质量分数和a点时溶液中溶质的质量.
 石灰石是主要修路材料之一,某兴趣小组用修路材料石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,该小组取石灰石20g,将一定质量的稀盐酸平均分5次加入其中,记录数据如下:
石灰石是主要修路材料之一,某兴趣小组用修路材料石灰石(杂质不与酸反应,也不溶于水)和稀盐酸反应制取二氧化碳,该小组取石灰石20g,将一定质量的稀盐酸平均分5次加入其中,记录数据如下:| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 剩余固体的质量/g | 17.8 | 15.6 | 13.4 | m | 13.4 |
(1)表中m=13.4;
(2)当20g石灰石完全反应时生成CO2的质量;
(3)Na2CO3溶液中溶质的质量分数和a点时溶液中溶质的质量.
