题目内容
19.在A+3B═2C+2D的反应中,14g A完全反应生成44g C和18g D,参加反应的B的质量为48g;若A的相对分子质量是28,则B的相对分子质量是32.分析 先根据质量守恒定律计算出14gA完全反应生成44gC和18gD时消耗B的质量,再根据方程式列比例式求出B的相对分子质量.
解答 解:由14克A完全反应生成44gC和18gD可知B的质量为:44g+18g-14g=48g,设B的相对分子质量为x,则:
A+3B=2C+2D
28 3x
14g 48g
$\frac{28}{3x}$=$\frac{14g}{48g}$,解得x=32.
故填:48g;32.
点评 解答本题容易出错的地方是在计算相对分子质量时与前面的系数有关.

练习册系列答案
相关题目
14.下列物质的性质与所对应的用途没有直接关系的是( )
| A. | 氧气的密度比空气略大--用于急救病人 | |
| B. | 氮气的性质稳定--作焊接保护气 | |
| C. | 稀有气体通电发光--制作电光源 | |
| D. | 干冰升华吸热--用于人工降雨 |
4.为确保生命安全,下列处理事故的方法不正确的是( )
| A. | 桌面上酒精灯内酒精洒出,着火燃烧,立即用湿抹布扑灭 | |
| B. | 厨房内管道煤气(主要成分是CO)泄漏,立即关闭阀门并开窗通风 | |
| C. | 进入深洞,燃着的火把熄灭立即停止前进,退出山洞 | |
| D. | 炒菜时油锅着火,立刻浇水灭火 |
11.下列有关水的说法不正确的( )
| A. | 用肥皂水可以检验硬水和软水 | |
| B. | 净化水的方法有电解、过滤、吸附和蒸馏等 | |
| C. | 合理施用农药、化肥,以减少水体污染 | |
| D. | 工业废水、生活污水处理达标后再排放 |
8.如图所示的微粒属于负二价阴离子的是( )
| A. | 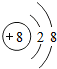 | B. | 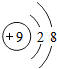 | C. |  | D. | 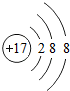 |
9.规范的操作是实验成功的保证.下列实验操作中,不符合操作规范的是( )
| A. | 给试管里的液体加热时,试管口对着没有人的方向 | |
| B. | 洒出的少量酒精在桌面上燃烧起来,立即用湿抹布盖灭 | |
| C. | 向试管内加液体时,将胶头滴管伸入试管内进行滴加 | |
| D. | 做铁丝在氧气中燃烧实验时,预先在集气瓶底铺一层细沙 |