题目内容
13.小明用碳酸钠溶液鉴别稀盐酸,氯化钠溶液和氯化钙熔液:分别取三种未知溶液样品于试管中,井将试管编号为A、B、C,然后用胶头滴管往三支试管中滴入一定量的碳酸钠溶液,观察到A中无明显现象,B中有白色沉淀产生,C中有气泡产生,则A中溶液的溶质为氯化钠;B中溶液的溶质为氯化钙.鉴别完成后,小明将三支队管中的物质全部倒人同一洁净的饶杯中,观察到烧杯底部有固体,上层为无色溶液.
【提出问题】烧杯上层溶液中的溶质是什么
【资料】氯化钙溶液显中性.
【猜想与假设】①氯化钠;②氯化钠和碳酸钠;③氯化钠和氯化氢;④氯化钠和氯化钙;③氯化钠、氯化氢和氯化钙.分析:小美同学认为上层溶液中不可能存在盐酸,其依据是盐酸与碳酸钙不能共存.
【设计与实验】
| 实验操作 | 实验现象 | 实验结论 | |
| 实验1 | 取上层清液样品于试管中,滴加酚酞溶液 | 试液变红色 | 猜想②不成立 |
| 实验2 | 取上层清液样品于试管中,加入碳酸钠溶液 | 产生白色沉淀 | 猜想④成立 |
分析 根据物质的性质进行分析,碳酸钠能与盐酸反应产生二氧化碳气体,碳酸钠溶液能与氢氧化钙溶液反应产生碳酸钙沉淀;根据盐酸的性质、碱性溶液能使无色的酚酞试液变红色,以及盐的性质来分析.
解答 解:氯化钠与碳酸钠不反应,故无明显现象,则A中含有氯化钠,B中有白色沉淀产生,氯化钙能与碳酸钠溶液反应生成碳酸钙沉淀,故B含有氯化钙;盐酸能与碳酸钠反应生成氯化钠、水和二氧化碳气体,有气泡产生;故C中物质是盐酸;故填:氯化钠;氯化钙;
【猜想与假设】题干信息可知,烧杯底部有固体存在,该固体是碳酸钙,碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,所以烧杯上层的溶液中一定不存在盐酸;故填:盐酸与碳酸钙不能共存;
【设计实验】①若猜想②成立,则因为其中含有碳酸钠而显碱性,滴加酚酞试液会变成红色,故填:试液变红色;
②若猜想④成立,则需要证明氯化钙的存在,可以加入碳酸钠溶液,若能产生白色沉淀,则证明猜想成立;故填:碳酸钠溶液;产生白色沉淀;
【拓展】如果将上层清液中的氯化钙除去,获得氯化钠溶液,可加入碳酸钠溶液,一直加到不再产生沉淀为止,故填:碳酸钠溶液.
点评 本题考查了常见物质成分的鉴别,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.分别用四种不同的澄清液体进行下列实验,其中一定发生化学变化的是( )
| A. | 加热--产生白色沉淀 | B. | 加入烧碱--温度升高 | ||
| C. | 加入木炭--褪色 | D. | 加入碳酸钙--产生气泡 |
18.下列各组物质的名称、俗称、化学式表示同一种物质的是( )
| A. | 氢氧化钠、纯碱、Na2CO3 | B. | 氯化银、食盐、NaCl | ||
| C. | 硫酸铜晶体、胆矾、CuSO4•5H2O | D. | 碳酸钙、生石灰、Ca(OH)2 |
5. 甲乙丙三种物质间通过一步反应能实现如图转化,下列选项中符合转化关系的是( )
甲乙丙三种物质间通过一步反应能实现如图转化,下列选项中符合转化关系的是( )
 甲乙丙三种物质间通过一步反应能实现如图转化,下列选项中符合转化关系的是( )
甲乙丙三种物质间通过一步反应能实现如图转化,下列选项中符合转化关系的是( )| 选项 | 甲 | 乙 | 丙 |
| A | NaOH | NaCl | NaNO3 |
| B | CuO | CuCl2 | Cu(OH)2 |
| C | Na2CO3 | CO2 | CaCO3 |
| D | H2O2 | H2O | O2 |
| A. | A | B. | B | C. | C | D. | D |
2.能一次性鉴别NaOH、Ca(OH)2、稀盐酸三种溶液的试剂是( )
| A. | 氯化铜溶液 | B. | 紫色石蕊试液 | C. | 酚酞试剂 | D. | 碳酸钠溶液 |
 A、B两图分别表示硫、铁丝在氧气中燃烧示意图
A、B两图分别表示硫、铁丝在氧气中燃烧示意图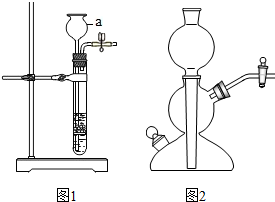 经过一年的学习,我们已经掌握了气体实验室制法的一些知识.
经过一年的学习,我们已经掌握了气体实验室制法的一些知识.