题目内容
17.在化学实验室里,常用如图所示的实验装置制取气体: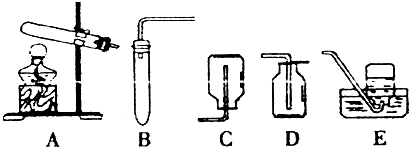
(1)用KMnO4制取O2,反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;实验结束后,某同学发现所用的水槽中的水变成了浅紫红色,从实验操作角度分析其主要原因是试管口没有放棉花团;
(2)实验室制取少量CO2时,应选用上图中的B(填序号)作发生装置,有关反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;如何检验D装置中是否已收集满CO2气体:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.
(3)如图是关于二氧化碳性质的微型实验装置图.试管中反应发生后,a处发生的变化现象是紫色变红色;b处有关反应的化学方程式中的挡板的主要作用是CaCO3+2HCl=CaCl2+H2O+CO2↑;挡板作用是防止二氧化碳气体逸散.
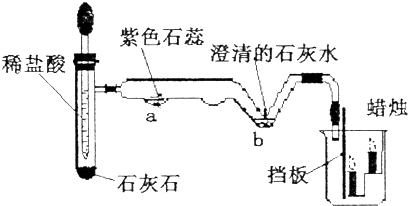
分析 制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热,加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;如图是关于二氧化碳性质的微型实验装置图.试管中反应发生后,a处发生的变化现象是:紫色变红色;b处的化学方程式是二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,配平即可;挡板作用是防止二氧化碳气体逸散.
解答 解:(1)高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;故答案为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;试管口没有放棉花团;
(2)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;故答案为:B;CaCO3+2HCl=CaCl2+H2O+CO2↑;将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;
(3)试管中反应发生后,a处发生的变化现象是:紫色变红色;b处的化学方程式是二氧化碳与氢氧化钙反应生成碳酸钙白色沉淀和水,配平即可;挡板作用是防止二氧化碳气体逸散;故答案为:紫色变红色;CaCO3+2HCl=CaCl2+H2O+CO2↑;挡板作用是防止二氧化碳气体逸散;
点评 本考点主要考查了注意事项、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. | 红磷在空气中燃烧,放出热量,生成大量白色烟雾 | |
| B. | 细铁丝在空气剧烈燃烧,火星四射,放出热量,生成黑色固体 | |
| C. | 木炭在氧气中燃烧,发出白光放出热量,产生能使澄清石灰水变浑浊的气体 | |
| D. | 硫在空气中燃烧,生成二氧化硫 |
| A. | O→+2 | B. | +2→O | C. | +4→O | D. | +4→+2 |
| A. |  比较二氧化碳的含量 | B. |  研究二氧化锰的催化作用 | ||
| C. |  区分硬水和软水 | D. |  配制氯化钠溶液 |
| A. | 单质中只含有一种元素,因此只含有一种元素的物质一定是单质 | |
| B. | 氧气是由氧元素组成的,所以制取氧气的反应物中一定含氧元素 | |
| C. | 在化合物里,正负化合价的代数和为零,所以在同一化合物中金属元素显正价,则非金属元素一定显负价 | |
| D. | 稀有气体元素的原子最外层电子数为8(氦除外),因此最外层电子数为8的微粒一定是稀有气体元素的原子 |
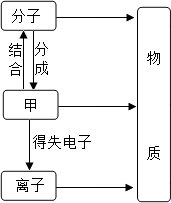 构成物质的粒子之间的关系如图所示,回答下列问题:
构成物质的粒子之间的关系如图所示,回答下列问题: