题目内容
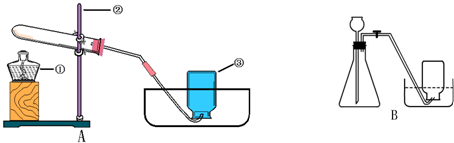
某同学设计下表所示实验,探究金属铜对过氧化氢(H2O2)分解速率的影响.
回答下列问题:
(1)仪器③的名称是 ;
(2)仪器②中实验的目的是 ;
(3)根据上述实验,可以得出的结论是 ;
(4)如果用本实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是(填序号) .
A.称量实验前铜丝网的质量 B.将实验后的铜丝网干燥、称重
C.向仪器中加入二氧化锰 D.将实验后的铜丝网插入H2O2溶液中,反复多次
(5)综上所述,催化剂必须能改变其他物质的化学反应速率,并且本身的 在反应前后都不发生变化.
| 操作 | 装置 | 现象 |
| 1、取一小块铜丝网,卷成筒形,固定在铜丝上. | 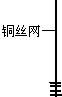 | / |
| 2、分别向①和②中注入15mL、30%的H2O2,并放入盛有热水的③中. | 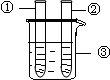 | 约1min后可观察到① 和②中都有少量气泡产生 |
| 3、把铜丝插入①中. | 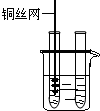 | ①中有大量气泡产生,约5min后不再有气泡产生;此时②中 仍然有少量气泡产生 |
(1)仪器③的名称是
(2)仪器②中实验的目的是
(3)根据上述实验,可以得出的结论是
(4)如果用本实验探究铜是不是H2O2分解的催化剂,需要对上述实验方案进行补充,其中必要的是(填序号)
A.称量实验前铜丝网的质量 B.将实验后的铜丝网干燥、称重
C.向仪器中加入二氧化锰 D.将实验后的铜丝网插入H2O2溶液中,反复多次
(5)综上所述,催化剂必须能改变其他物质的化学反应速率,并且本身的
考点:影响化学反应速率的因素探究,催化剂的特点与催化作用
专题:科学探究
分析:(1)根据常见仪器的名称和用途进行解答;
(2)只有对比才能够鉴别出铜网的作用,由此可以得出仪器②的作用;
(3)根据实验现象可以总结归纳出实验结论;
(4)根据催化剂的定义可以知道,催化剂在反应前后质量和化学性质不变,可以据此解题.(5)根据催化剂在反应前后的质量和化学性质不变回答.
(2)只有对比才能够鉴别出铜网的作用,由此可以得出仪器②的作用;
(3)根据实验现象可以总结归纳出实验结论;
(4)根据催化剂的定义可以知道,催化剂在反应前后质量和化学性质不变,可以据此解题.(5)根据催化剂在反应前后的质量和化学性质不变回答.
解答:解:(1)仪器③的名称烧杯;
(2)仪器①和仪器②加入的过氧化氢的浓度相同,但是仪器②中没有加入铜网,所以仪器②所起的作用是对照作用
(3)根据实验现象:①中有大量气泡产生,约5min后不再有气泡产生;此时②中仍然有少量气泡产生.可以得出金属铜对过氧化氢溶液分解速率有加快的作用;
(4)虽然从实验现象中可以看出金属铜对过氧化氢溶液分解速率有加快的作用,但是不知道铜丝在反应前后的质量和化学性质是否改变,要对铜丝的质量和化学性质进行实验.所以需要对上述实验方案进行补充称量实验前铜丝网的质量;将实验后的铜丝网干燥、称重;将实验后的铜丝网插入AgNO3溶液中;而加入二氧化锰与该实验无关,故选ABD.(5)催化剂必须能改变其他物质的化学反应速率,并且本身的质量和化学性质在反应前后都不发生变化.
故答案为:(1)烧杯;
(2)和①作对比(对照);
(3)否,铁丝也有可能加快H2O2的分解(或铁丝也有可能起催化作用)
(4)ABD(5)质量和化学性质
(2)仪器①和仪器②加入的过氧化氢的浓度相同,但是仪器②中没有加入铜网,所以仪器②所起的作用是对照作用
(3)根据实验现象:①中有大量气泡产生,约5min后不再有气泡产生;此时②中仍然有少量气泡产生.可以得出金属铜对过氧化氢溶液分解速率有加快的作用;
(4)虽然从实验现象中可以看出金属铜对过氧化氢溶液分解速率有加快的作用,但是不知道铜丝在反应前后的质量和化学性质是否改变,要对铜丝的质量和化学性质进行实验.所以需要对上述实验方案进行补充称量实验前铜丝网的质量;将实验后的铜丝网干燥、称重;将实验后的铜丝网插入AgNO3溶液中;而加入二氧化锰与该实验无关,故选ABD.(5)催化剂必须能改变其他物质的化学反应速率,并且本身的质量和化学性质在反应前后都不发生变化.
故答案为:(1)烧杯;
(2)和①作对比(对照);
(3)否,铁丝也有可能加快H2O2的分解(或铁丝也有可能起催化作用)
(4)ABD(5)质量和化学性质
点评:此题属于实验探究题,解题时要理清思路,特别注意实验过程中的细节,另外要注意对比试验的设计意图.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
下列物质中,属于纯净物的是( )
| A、凉茶 | B、可乐 | C、苹果醋 | D、液氧 |
下列说法正确的是( )
| A、氧化反应一定是化合反应 |
| B、分子可分、原子不可分 |
| C、含氧元素的化合物是氧化物 |
| D、春天闻到花香,说明分子是不断运动的 |
在搪瓷面盆表面烧制一层搪瓷的目的是( )
| A、增大硬度,防止撞坏 |
| B、增大美观 |
| C、防止铁生锈且美观 |
| D、杀菌消毒 |
人体缺铁会造成贫血,缺碘会造成甲状腺肿大,缺钙会造成骨质疏松.这里的铁、碘、钙是指( )
| A、单质 | B、分子 |
| C、金属离子 | D、元素 |
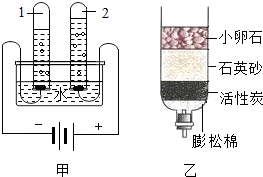 水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.
水是生命之源,“珍惜水、节约水、保护水”是每个公民的义务和责任.