题目内容
8.某实验小组为研究碳酸钠和碳酸氢钠混合物的组成做了以下实验:充分加热10.0g样品至恒重,剩余固体质量为6.9g.查阅资料已知:碳酸氢钠受热易分解生成碳酸钠、水和二氧化碳;碳酸钠受热不易分解.计算:
(1)生成二氧化碳的质量.
(2)混合物中碳酸钠的质量分数.
分析 加热碳酸钠和碳酸氢钠的混合物时,碳酸钠不分解,碳酸氢钠不稳定,加热时分解生成碳酸钠、二氧化碳和水,利用差量法,结合反应的化学方程式,即可解答.
解答 解:
设:二氧化碳的质量为x;NaHCO3的质量为y
2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$ Na2CO3+H2O+CO2↑ 固体△m
168 106 44 62
y x 10 g-6.9g=3.1g
$\frac{168}{y}=\frac{44}{x}=\frac{62}{3.1g}$
x=2.2 g
y=8.4 g
10 g-8.4 g=1.6 g
Na2CO3的质量分数为:$\frac{1.6g}{10g}$×100%=16%
答:二氧化碳的质量为2.2 g,碳酸钠的质量分数是16%.
点评 本题考查混合物的计算,题目难度不大,注意根据碳酸氢钠不稳定的性质,利用差量法计算.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
19.下列各组气体中,均能用氢氧化钠固体干燥的一组是( )
| A. | O2、CO、CO2 | B. | H2、O2、HCl | C. | H2、SO2、CO | D. | H2、O2、CO |
16.下列四个图象分别对应四个变化过程,其中正确的是( )
| A. | 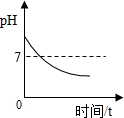 服用胃舒平[主要成分Al(OH)3]治疗胃酸过多(胃液pH随时间变化图) | |
| B. | 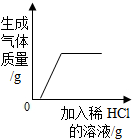 向氢氧化钠和碳酸钠的混合溶液中加入稀盐酸溶液直至过量 | |
| C. | 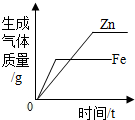 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应 | |
| D. | 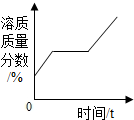 将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出 |
12.两会期间,环保问题成为年度热议的焦点,下列做法,不符合“低碳环保”的理念是( )
| A. | 生活中纸张双面使用 | |
| B. | 绿色出行,骑行自行车上学 | |
| C. | 减少或不使用一次性木筷 | |
| D. | 为了促进工业发展,大力发展火力发电 |
10.氢氧化钙是一种建筑材料,它的俗名是( )
| A. | 生石灰 | B. | 石灰水 | C. | 熟石灰 | D. | 大理石 |