题目内容
6.化学与生活、生产息息相关,请运用化学知识回答以下问题.(1)铝制品抗腐蚀性能很好,原理是4Al+3O2=2Al2O3(用化学方程式表示).
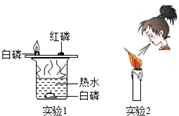
(2)若装白磷的储罐起火,可以用水灭火,也可以用沙土填埋灭火.其中用沙土填埋灭火的原理是隔绝白磷与空气接触.
(3)电池中含有铅、镍、镉、汞等金属,随意丢弃废旧电池,会造成水体和土壤污染,威胁人类健康.回收废旧电池的重要意义是AC
A.节约金属资源 B.增加金属产量 C.减少环境污染
(4)要对生活中常见的Al、Ag、Cu三种金属活动性顺序进行探究,下列所选试剂组不可取的是②.
①Al、Ag、CuSO4 溶液 ②Cu、Ag、Al2(SO4)3溶液 ③Cu、Al2(SO4)3溶液、AgNO3溶液.
分析 (1)根据金属铝的化学性质进行分析解答;
(2)根据灭火的方法考虑;
(3)歌女回收废旧金属的意义进行分析解答即可;
(4)根据金属活动顺序进行思考,Al、Ag、Cu这三种金属的金属活动性由强到弱的顺序为Al>Cu>Ag.在金属活动顺序表中,前边的金属可以把后边的金属从其盐溶液中置换出来,所以可以选择相应的金属和盐溶液进行反应来证明这三种金属的活动性强弱.
解答 解:
(1)铝在空气中能与氧气反应,生成一层致密的氧化铝薄膜,从而阻止了内部的铝进一步氧化;反应的化学方程式为:4Al+3O2=2Al2O3.
(2)用沙土填埋灭火的原理是隔绝了空气,使白磷不能与氧气接触.
(3)回收废旧电池能节约金属资源、减少环境污染.故填:AC.
(4)①Al、Ag、CueSO4溶液这三种物质中,Al与CuSO4溶液反应,证明铁的活动性比铜强,Ag与CuSO4溶液不能反应,证明铜比银的活动性强.所以,所选试剂组可行;
②、因为铁的活动性在三种金属中最强,所以Cu,Ag都不能和Al2(SO4)3溶液反应,得不出Cu,Ag的活动性强弱,所以此试剂组不可行;
③、Cu、Al2(SO4)3溶液、AgNO3溶液.这三种物质中,Cu与Al2(SO4)3溶液不反应,证明铝的活动性比铜强,Cu与AgNO3溶液能反应,证明铜比银的活动性强,可以证明三种金属的活动性强弱,此试剂组可行.
故答案为:
(1)4Al+3O2=2Al2O3.
(2)隔绝白磷与空气接触;
(3)AC;
(4)②
点评 掌握金属锈蚀的因素以及金属的性质、回收废旧金属的意义是正确解答本题的关键.要会利用金属活动顺序表设计实验,去验证金属的活动性强弱.氢前边的金属会与酸反应,但氢后边的金属不会与酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.但也要注意,与金属反应酸一般是指稀硫酸和盐酸,不包括浓硫酸和硝酸.

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案| 温度/℃ | 10 | 30 | 50 | 60 | |
| 溶解度/g | 氢氧化钙 | 0.18 | 0.15 | 0.12 | 0.11 |
| 硝酸钾 | 20.9 | 45.8 | 85.5 | 110 | |
| A. | 将50℃的氢氧化钙饱和溶液降温会析出晶体 | |
| B. | 30℃硝酸钾的饱和溶液溶质的质量分数为45.8% | |
| C. | 50℃时不可能配得溶质质量分数相等的硝酸钾、氢氧化钙两种溶液 | |
| D. | 硝酸钾的饱和溶液升高温度后还可以继续溶解硝酸钾固体 |
| A. | BaCl2、HNO3、H2SO4 | B. | Na2CO3、HCl、KOH | ||
| C. | NaCl、CuSO4、HNO3 | D. | Mg(NO3)2、NaCl、NaOH |
| A. | 提倡使用清洁能源 | B. | 加高烟窗排放工业废气 | ||
| C. | 不焚烧垃圾 | D. | 骑自行车出行 |
| A. | 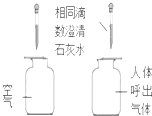 比较二氧化碳的含量 | |
| B. | 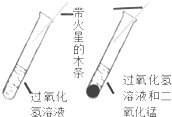 研究二氧化锰的催化作用 | |
| C. |  区分硬水和软水 | |
| D. | 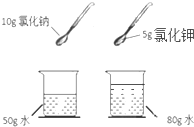 常温下比较氯化钠和氯化钾的溶解能力 |
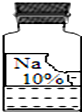 实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示)
实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示)小强和小华同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是A
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3.
Ⅱ.Na2CO3和NaHCO3的水溶液都呈碱性.
Ⅲ.室温(20℃)时,测定四种物质的溶解度数据如表:
| 物 质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
【作出猜想】①可能是NaCl;②可能是Na2CO3;③可能是NaOH.
【实验探究】
(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH>7,则这瓶试剂不可能是NaCl溶液.
(2)小强为了检验该溶液是剩余两个猜想中的哪一个,他又进行了如表实验.
| 实验步骤 | 实验现象 | 结论及化学方程式 |
| 取少量溶液于试管中,滴加BaCl2溶液. | 产生白色沉淀 | 猜想②正确. 反应的化学方程式:BaCl2+Na2CO3=BaCO3+NaCl. |