题目内容
20.M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动.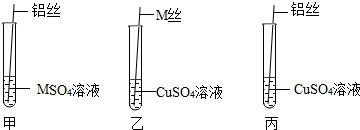
(1)【提出问题】M、铜、铝的金属活动性顺序是怎样的?
(2)【猜想与假设】小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是M>Al>Cu.
(3)【设计与实验一】小莉取M丝、铜丝、铝丝和编号为①、②、③的3支试管,进行如表的实验(试管中均盛有体积相同、溶质质量分数也相同的稀盐酸),根据实验现象,完成表中的实验结论:
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu:M>Al |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 | Al>M>Cu |
(5)【设计与实验二】为了进一步探究三种金属的活动性顺序,同学们取粗细相同,打磨干净的M丝、铝丝及相关溶液,又进行了如图所示的实验:
①试管乙中观察到的现象是M表面出现一层红色物质.
②试管丙中反应的化学方程式为2Al+3CuSO4=Al2(SO4)3+3Cu.
(6)【交流与表达】同学们经讨论后认为该实验可以优化,去掉试管丙(填试管编号)中的实验,也可以得出正确的结论.
分析 【提出问题】根据其余两种猜想推断第三种猜想;
【设计与实验一】根据金属与酸反应的剧烈程度进行分析;
【交流与表达】根据铝和空气中的氧气反应会生成致密的氧化铝薄膜进行分析;
【设计与实验二】(1)根据M的金属活动性大于铜的金属活动性进行分析;
(2)根据铝和硫酸铜反应生成硫酸铝和铜进行分析;
【交流与表达】根据甲、乙、丙三个实验得出的金属活动性顺序进行分析;
【评价与反思】根据金属会与酸、盐、氧气等物质反应进行分析.
解答 解:【提出问题】通过分析小敏、小强同学的猜想可知,我的猜想是M>Al>Cu;
【设计与实验一】金属越活泼,与酸反应生成氢气的反应越剧烈,所以
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| 刚开始的现象 | 有少量气泡产生 | 无气泡 | 无气泡 | M>Cu,M>Al |
| 几分钟后的现象 | 有少量气泡产生 | 无气泡 | 有大量气泡产生 | Al>M>Cu |
【设计与实验二】(1)M的金属活动性大于铜的金属活动性,所以试管乙中观察到的现象是:M表面出现一层红色物质;
(2)铝和硫酸铜反应生成硫酸铝和铜,化学方程式为:2Al+3CuSO4=Al2(SO4)3+3Cu;
【交流与表达】甲实验可以验证铝比M活泼,乙实验可以证明M比铜活泼,所以三种金属的活动性顺序是Al>M>Cu,所以去掉试管丙中的实验,也可以得出正确的结论;
故答案为:【提出问题】M>Al>Cu;
【设计与实验一】
| 实验操作 | M丝插入试管①中 | 铜丝插入试管②中 | 铝丝插入试管③中 | 实验结论 |
| M>Al | ||||
| Al>M>Cu |
【设计与实验二】(1)M表面出现一层红色物质;
(2)2Al+3CuSO4=Al2(SO4)3+3Cu;
【交流与表达】丙;
点评 验证三种金属活动性强弱关系时,通常采取“三取中”即:取中间金属单质与两端的金属的盐溶液反应或取中间金属的盐溶液与两端金属的单质反应.

练习册系列答案
相关题目
19.在化学反应A+2B═C+3D中,2gA与4.1gB恰好完全反应生成5.5gC,若有1.5gD生成时,反应物A的质量是( )
| A. | 0.5g | B. | 4.5g | C. | 5.6g | D. | 5g |
15.下列叙述中,前者属于物质的化学性质,后者属于物质的物理性质的是( )
| A. | 镁带在空气中燃烧;酒精挥发 | |
| B. | 二氧化硫具有刺激气味;氯气有毒 | |
| C. | 氧气能支持燃烧;水在降温时会结冰 | |
| D. | 蜡烛受热熔化;液氧是淡蓝色的液体 |
5.重庆的火锅全国闻名.“纸火锅”是用纸制的容器代替金属容器盛放汤料,用酒精加热.酒精燃烧时,“纸火锅”不燃烧,原因是( )
| A. | 纸不是可燃物 | B. | 汤料降低了纸的着火点 | ||
| C. | 汤料有吸热降温的作用 | D. | 纸没有与氧气接触 |
9.如表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水)
(1)20℃时,NaCl的溶解度是36g.
(2)根据表内数据可知,KNO3和NaCl溶解度相等的温度取值范围是20℃~30℃.
(3)如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答:
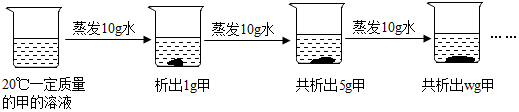
①蒸发前原溶液是不饱和(填“饱和”和“不饱和”)溶液.
②w的数值是5g.
③依据上述实验,你认为甲的溶解度随温度变化的趋势是C(填编号).
A.随温度升高而增大B.随温度升高而减小C.无法判断.
| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3 | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
(2)根据表内数据可知,KNO3和NaCl溶解度相等的温度取值范围是20℃~30℃.
(3)如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,请回答:

①蒸发前原溶液是不饱和(填“饱和”和“不饱和”)溶液.
②w的数值是5g.
③依据上述实验,你认为甲的溶解度随温度变化的趋势是C(填编号).
A.随温度升高而增大B.随温度升高而减小C.无法判断.
10.日本某一材料研究所的科学家发明了一种“碳纳米管温度计”,这种温度计被认定为是目前世界上最小的温度计.研究人员在长约 10-6m,直径为 10-7m 的碳纳米管中充入液态的金属镓.当温度升高时,管中稼就会膨胀,通过电子显微镜就能读取温度值.这种温度计测量的范围可从30℃到490℃,并且精确度较高,可用于检查电子线路是否异常、测量毛细血管的温度等许多方面.根据以上信息判断下列推测中正确的是( )
| A. | 碳纳米管的体积在 10℃至 500℃之间随温度变化很小,可忽略不计 | |
| B. | 金属镓的熔点、沸点都很低 | |
| C. | 在 30℃至 490℃之间金属镓的体积与温度变化呈正比 | |
| D. | 金属镓的体积在 30℃至 490℃之间随温度变化很小,可忽略不计 |