题目内容
8.氧化铜粉末中加入足量的稀硫酸的实验现象是粉末溶解,溶液变成蓝色,化学反应方程式是CuO+H2SO4═CuSO4+H2O;继续滴加烧碱溶液的实验现象是产生蓝色沉淀,化学方程式是2NaOH+CuSO4═Na2SO4+Cu(OH)2↓;再滴加盐酸时的实验现象是沉淀溶解,溶液变成蓝色,化学方程式是Cu(OH)2+2HCl═CuCl2+2H2O.分析 氧化铜和稀硫酸反应生成硫酸铜和水,硫酸铜和氢氧化钠反应生成氢氧化铜沉淀和硫酸钠,氢氧化铜和稀盐酸反应生成氯化铜和水.
解答 解:氧化铜粉末中加入足量的稀硫酸的实验现象是粉末溶解,溶液变成蓝色,化学反应方程式是:CuO+H2SO4═CuSO4+H2O;
继续滴加烧碱溶液的实验现象是产生蓝色沉淀,化学方程式是:2NaOH+CuSO4═Na2SO4+Cu(OH)2↓;
再滴加盐酸时的实验现象是沉淀溶解,溶液变成蓝色,化学方程式是:Cu(OH)2+2HCl═CuCl2+2H2O.
故填:粉末溶解,溶液变成蓝色;CuO+H2SO4═CuSO4+H2O;产生蓝色沉淀;2NaOH+CuSO4═Na2SO4+Cu(OH)2↓;沉淀溶解,溶液变成蓝色;Cu(OH)2+2HCl═CuCl2+2H2O.
点评 本题主要考查物质的性质,只有掌握了各种物质的性质,才能够判断物质之间相互转化时的反应物和生成物,从而可以进行各方面的判断.

练习册系列答案
 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案
相关题目
14.某同学对若干块矿石样品中的碳酸钙的质量分数进行检测,采用了以下的办法:取用8g这种石灰石样品,把40g稀盐酸分四次加入,测量过程所得数据见下表(已知石灰石样品中含有的杂质不溶于水,不与盐酸反应).请计算:
(1)8g的石灰石样品中含有杂质1.2克?
(2)如表中m的数值应为3?
(3)稀盐酸的质量分数是多少?
| 序号 | 加入稀盐酸质量(g) | 剩余固体质量(g) |
| 第1次 | 10 | 5.5 |
| 第2次 | 10 | m |
| 第3次 | 10 | 1.2 |
| 第4次 | 10 | 1.2 |
(2)如表中m的数值应为3?
(3)稀盐酸的质量分数是多少?
13.下列有关现象的描述正确的是( )
| A. | 少量面粉放入足量水中充分搅拌,能形成均一、稳定的溶液 | |
| B. | 木炭在氧气中燃烧发出白光,生成黑色固体,放出热量 | |
| C. | 将Cu(OH)2加入到滴有酚酞试液的蒸馏水中,溶液显红色 | |
| D. | 把氢氧化钠溶液中逐滴加入氯化铁溶液中,产生红褐色沉淀 |
20.香料化学家已经开发出多种脂类人工香料,如丁酸甲酯(化学式为C5H10O2)具有苹果香味.下列有关丁酸甲酯的说法正确的是( )
| A. | 丁酸甲酯属于氧化物 | |
| B. | 丁酸甲酯由5个碳原子、10个氢原子和2个氧原子构成 | |
| C. | 丁酸甲酯中碳元素、氢元素和氧元素的质量比为30:5:16 | |
| D. | 丁酸甲酯的每个分子由17个原子构成 |
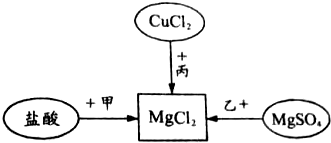
 在宏观、微观和符号之间建立联系是化学学科的特点.
在宏观、微观和符号之间建立联系是化学学科的特点.