题目内容
14.根据初中化学酸、碱、盐的知识可知,将蓝色的硫酸铜溶液与氢氧化钠溶液混合后,可得到蓝色沉淀,其反应的化学方程式为CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.小军和小亮分别进行如下硫酸铜与氢氧化钠反应的性质实验探究:
(1)小军将上述有蓝色沉淀的浊液进行加热,发现沉淀变黑;
(2)小亮做这个实验时,在试管中倒入2mL CuSO4溶液,再加入一定量NaOH溶液,结果并没有得到蓝色的沉淀,而是浅绿色的沉淀;将此浊液加热直至沸腾,仍然观察不到有黑色的物质生成.
(思 考)①黑色物质是什么?②浅绿色的沉淀是什么?
(资料卡)
①氢氧化铜加热可以分解成2种氧化物;
②Cu4(OH)6SO4是一种浅绿色物质,溶解度极小,可溶于酸液;
③反应物的量不同,则生成物可能有所不同.
(3)通过查找资料卡得知:蓝色沉淀加热生成一种黑色物质的化学方程式为Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O,
浅绿色的沉淀是Cu4(OH)6SO4,其化学名称是碱式硫酸铜,生成该沉淀的化学方程式为:
4CuS04+6NaOH═Cu4(OH)6S04↓+3Na2SO4.
(实验探究)
(4)证明该浅绿色沉淀中含有S042-,他俩共同设计如下方案:
| 操作步骤 | 实验现象 | 结论 |
| ①将浅绿色的浊液过滤,并把得到的浅绿色沉淀用蒸馏水多次洗涤,直至取最后一次洗涤液,滴加BaCl2溶液. | 无现象 | 沉淀表面无Na2SO4残留(附着)或者已经洗净 |
| ②用稀盐酸溶解浅绿色沉淀,再滴加BaCl2溶液. | 有大量白色沉淀生成 | 沉淀中含有SO42- |
分析 根据硫酸铜溶液与氢氧化钠溶液反应生成氢氧化铜沉淀和硫酸钠解答;
(3)根据氢氧化铜加热分解生成氧化铜和水解答;根据质量守恒定律,化学反应前后原子的种类和数目不变解答;
(4)根据BaCl2溶液和硫酸钠反应,生成硫酸钡沉淀解答.
解答 解:
蓝色硫酸铜溶液与氢氧化钠溶液反应生成氢氧化铜沉淀和硫酸钠,其反应的化学方程式为:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4;
(3)氢氧化铜加热分解生成氧化铜和水,化学方程式为:Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O;浅绿色的沉淀是Cu4(OH)6SO4,其化学名称是碱式硫酸铜;
根据质量守恒定律,化学反应前后原子的种类和数目不变,生成该沉淀的化学方程式为:4CuS04+6NaOH═Cu4(OH)6S04↓+3Na2SO4 ;
(4)①将浅绿色的浊液过滤,并把得到的浅绿色沉淀用蒸馏水多次洗涤,直至取最后一次洗涤液,滴加BaCl2溶液.无现象,说明无Na2SO4残留(附着)或者已经洗净;
②用稀盐酸溶解浅绿色沉淀,再滴加BaCl2溶液.有大量白色沉淀生成,沉淀中含有SO42-;
多次洗涤沉淀的目的是:将沉淀表面附着的Na2SO4溶液洗净,防止其中的SO42-干扰实验;
稀盐酸溶解浅绿色沉淀的化学方程式为:Cu4(OH)6SO4+6HCl═CuSO4+3CuCl2+6H2O.
答案:蓝色;CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
(3)Cu(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CuO+H2O; 碱式硫酸铜;3Na2SO4
(4)
| 作步骤 | 实验现象 | 结论 |
| ①将浅绿色的浊液过滤,并把得到的浅绿色沉淀用蒸馏水多次洗涤,直至取最后一次洗涤液,滴加BaCl2溶液. | 无现象 | 沉淀表面 无Na2SO4残留(附着)或者已经洗净 |
| ②用稀盐酸溶解浅绿色沉淀,再滴加BaCl2溶液. | 有大量白色沉淀生成 | 沉淀中含有 SO42- |
Cu4(OH)6SO4+6HCl═CuSO4+3CuCl2+6H2O
点评 有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;关于对实验设计方案的评价,要在两个方面考虑,一是方案是否可行,能否达到实验目的;二是设计的方法进行比较,那种方法更简便.本考点主要出现在实验题中.

| A. | -2 | B. | +2 | C. | +6 | D. | +4 |
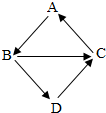 如图中A、B、C、D均为初中阶段常见物质,它们转化关系用如图所示.下列说法中错误的是( )
如图中A、B、C、D均为初中阶段常见物质,它们转化关系用如图所示.下列说法中错误的是( )| A. | 若A、C、D均为白色固体,则B→D的反应可能是中和反应 | |
| B. | 若B为红色固体单质,则D可能为绿色固体 | |
| C. | 若B、C、D为气体,则A可能为常见的液体 | |
| D. | 若C、D为元素组成相同的氧化物,则A可能为氧气 |
| A. | NaOH、KCl、KNO3、FeCl3 | B. | Na2SO4、BaCl2、KNO3、NaCl | ||
| C. | K2SO4、Na2CO3、BaCl2、稀HNO3 | D. | Na2CO3、稀H2SO4、稀HCl、NaNO3 |