题目内容
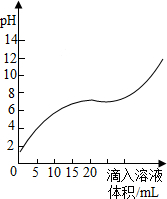 如图是盐酸和氢氧化钠溶液用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.
如图是盐酸和氢氧化钠溶液用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线.(1)根据曲线判断,该反应是将
(2)当滴入溶液的体积为10mL时,所得溶液中的溶质为
考点:中和反应及其应用
专题:常见的酸 酸的通性
分析:(1)当溶液的pH<7时,溶液显酸性,当溶液的pH>7时,溶液显碱性,当溶液的pH=7时,溶液显中性;
(2)根据盐酸和氢氧化钠的反应原理以及图象数据来回答.
(2)根据盐酸和氢氧化钠的反应原理以及图象数据来回答.
解答:解:
(1)根据图象,在反应未进行时,溶液的pH=1,为强酸性溶液,所以该曲线反应是将氢氧化钠溶液滴入盐酸中;
(2)盐酸和氢氧化钠的反应原理是:HCl+NaOH=NaCl+H2O,滴入氢氧化钠溶液的体积为10mL时,溶液仍为酸性,所以是氢氧化钠只和部分盐酸反应,所得溶液中的溶质有生成的氯化钠也有剩余的盐酸.
答案:
(1)氢氧化钠溶液;盐酸;
(2)NaCl、HCl;
(1)根据图象,在反应未进行时,溶液的pH=1,为强酸性溶液,所以该曲线反应是将氢氧化钠溶液滴入盐酸中;
(2)盐酸和氢氧化钠的反应原理是:HCl+NaOH=NaCl+H2O,滴入氢氧化钠溶液的体积为10mL时,溶液仍为酸性,所以是氢氧化钠只和部分盐酸反应,所得溶液中的溶质有生成的氯化钠也有剩余的盐酸.
答案:
(1)氢氧化钠溶液;盐酸;
(2)NaCl、HCl;
点评:本题考查酸碱中和滴定,正确分析图象是解本题关键,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
含氮元素的氧化物中,氮元素呈+4价的是( )
| A、NO |
| B、N2O3 |
| C、NO2 |
| D、N2O5 |
下列实验现象描述正确的是( )
| A、打开盛有浓盐酸的瓶盖,瓶口出现白烟 |
| B、铜丝浸入硝酸银溶液中,溶液由蓝色变无色 |
| C、氯化铵和熟石灰混合研磨,闻到刺激性气味 |
| D、点燃棉线,闻到烧焦羽毛的气味 |
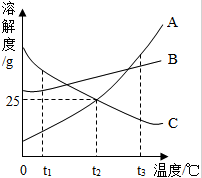 根据溶液的知识回答下列问题.
根据溶液的知识回答下列问题.
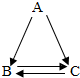 如图所示,A、B、C都是我们学习过的物质,其中C是常用于光合作用和灭火的气体,且B与C的组成元素相同.请按要求回答问题:
如图所示,A、B、C都是我们学习过的物质,其中C是常用于光合作用和灭火的气体,且B与C的组成元素相同.请按要求回答问题: