题目内容
2.某同学向50g过氧化氢溶液中加入二氧化锰制取气,生成O21.6g,该同学所用过氧化氢溶液的溶质质量分数是多少?分析 根据生成的氧气的质量和对应的过氧化氢分解的化学方程式求算过氧化氢的质量,最后求算所用过氧化氢溶液中溶质的质量分数.
解答 解:设生成1.6g氧气所消耗的过氧化氢的质量为x.
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{32}$=$\frac{x}{1.6g}$
x=3.4g
则该同学所用过氧化氢溶液的溶质质量分数是$\frac{3.4g}{50g}$×100%=6.8%.
答:该同学所用过氧化氢溶液的溶质质量分数是为6.8%.
点评 根据生成物直接求算反应物,过程很简单,但是要注意解答过程的相对分子质量以及计算的准确性.

练习册系列答案
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案
相关题目
12.下列粒子结构示意图中,表示阴离子的是( )
| A. |  | B. | 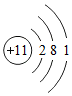 | C. |  | D. | 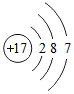 |
17.下列反应不能发生的是( )
| A. | CO2+NaOH | B. | SiO2+NaOH | C. | SO2+KOH | D. | SO2+Cu(OH)2 |
4.下列四种粒子的结构示意图表示元素周期表中在同一横行的原子的是( )
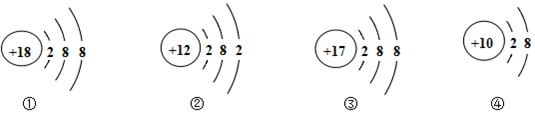

| A. | ①④ | B. | ①③④ | C. | ①② | D. | ①②③ |
11.正确的实验操作是科学探究成功的基础.下列操作正确的是( )
| A. |  | B. | 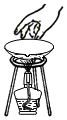 | C. | 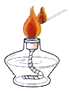 | D. | 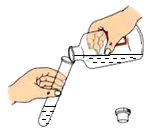 |
8.善于用化学的眼光看世界,能够提高我们的科学素养.你认为下列变化事实和相应的解释不一致的是( )
| 事实 | 解释 | |
| A | 装有相同体积空气和水的注射器,空气容易压缩 | 分子之间有间隔 |
| B | 氧气可供人呼吸,一氧化碳有毒 | 构成物质的分子不同,物质的性质不同 |
| C | 水通电后生成氢气和氧气 | 在化学变化中分子可以再分 |
| D | 温度计中的水银(汞)热胀冷缩 | 原子本身的大小发生了改变 |
| A. | A | B. | B | C. | C | D. | D |
9.下列各组物质混合后,溶液质量不会变化的是( )
| A. | 氢氧化钾溶液和盐酸 | B. | 稀硫酸和氯化钡溶液 | ||
| C. | 碳酸钠溶液和盐酸 | D. | 氧化铜和稀硫酸 |