题目内容
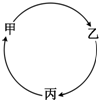 甲、乙、丙三种物质有如右图所示的转化关系.
甲、乙、丙三种物质有如右图所示的转化关系.Ⅰ.若甲、乙、丙依次是氢气、水、硫酸.?
(1)写出丙→甲的化学方程式:
H2SO4+Zn=ZnSO4+H2↑
H2SO4+Zn=ZnSO4+H2↑
.(2)乙→丙时所需另一种反应物中,一定含有氧元素和
硫
硫
元素.?Ⅱ.若甲为氢氧化钠,丙为硫酸钠.?
(3)乙可以是
碳酸钠
碳酸钠
.?Ⅲ.已知难溶性的碱受热会分解生成相应的金属氧化物和水.若甲是氧化铜,乙的水溶液呈蓝色,丙属于碱类.
(4)甲→乙还需要的试剂可以是
硫酸
硫酸
.?(5)写出乙→丙的化学方程式:
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
,属于复分解
复分解
反应.分析:(1)根据金属与酸反应产生氢气,写出反应的方程式;(2)根据质量守恒定律分析;(3)根据甲为氢氧化钠,丙为硫酸钠的性质分析乙可能的物质等;
(4)若甲是甲是氧化铜,甲在一定条件下转换为乙,乙的溶液呈蓝色,则乙为酸,酸与氧化铜反应生成带有铜离子的盐,则甲→乙还需要的试剂可以是盐酸或硫酸等;(5)根据甲是氧化铜,可有难溶性的碱丙氢氧化铜受热分解生成,则乙→丙可通过可溶性的铜盐与可溶性的碱反应制取,选择物质写出反应的方程式
(4)若甲是甲是氧化铜,甲在一定条件下转换为乙,乙的溶液呈蓝色,则乙为酸,酸与氧化铜反应生成带有铜离子的盐,则甲→乙还需要的试剂可以是盐酸或硫酸等;(5)根据甲是氧化铜,可有难溶性的碱丙氢氧化铜受热分解生成,则乙→丙可通过可溶性的铜盐与可溶性的碱反应制取,选择物质写出反应的方程式
解答:解:(1)金属与酸反应产生氢气,所以用锌与硫酸反应可以制取氢气,所以甲→乙的化学方程式是:H2SO4+Zn=ZnSO4+H2↑;
(2)由于水中含有氢、氧元素,并且氢、氧原子的个数比为;2:1,在硫酸中含有氢、硫、氧三种元素,且氢氧原子的个数比是1:2,由质量守恒定律可知,乙→丙时所需另一种反应物中,一定含有硫元素和氧元素;
(3)若甲为氢氧化钠,氢氧化钠与二氧化碳反应生成碳酸钠,乙可以是碳酸钠,碳酸钠与硫酸反应生成硫酸钠、水、二氧化碳;所以,乙可能是碳酸钠;
(4)若甲是氧化铜,氧化铜是不溶于水的金属氧化物,可以用酸来溶解,所以甲→乙还需要的试剂可以是硫酸,乙为硫酸铜;
(5)由题意可知,甲是氧化铜,可有难溶性的碱丙氢氧化铜受热分解生成,则乙→丙可通过可溶性的铜盐与可溶性的碱反应制取,所以反应物可以是硫酸铜和氢氧化钠,生成物是氢氧化铜沉淀和硫酸钠,用观察法配平,所以反应的方程式是:CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;两种化合物相互交换成分生成两种新的化合物的反应类型是置换反应.
故答案为:(1)H2SO4+Zn=ZnSO4+H2↑;(2)硫;(3)碳酸钠;(4)硫酸;(5)CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;复分解.
(2)由于水中含有氢、氧元素,并且氢、氧原子的个数比为;2:1,在硫酸中含有氢、硫、氧三种元素,且氢氧原子的个数比是1:2,由质量守恒定律可知,乙→丙时所需另一种反应物中,一定含有硫元素和氧元素;
(3)若甲为氢氧化钠,氢氧化钠与二氧化碳反应生成碳酸钠,乙可以是碳酸钠,碳酸钠与硫酸反应生成硫酸钠、水、二氧化碳;所以,乙可能是碳酸钠;
(4)若甲是氧化铜,氧化铜是不溶于水的金属氧化物,可以用酸来溶解,所以甲→乙还需要的试剂可以是硫酸,乙为硫酸铜;
(5)由题意可知,甲是氧化铜,可有难溶性的碱丙氢氧化铜受热分解生成,则乙→丙可通过可溶性的铜盐与可溶性的碱反应制取,所以反应物可以是硫酸铜和氢氧化钠,生成物是氢氧化铜沉淀和硫酸钠,用观察法配平,所以反应的方程式是:CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;两种化合物相互交换成分生成两种新的化合物的反应类型是置换反应.
故答案为:(1)H2SO4+Zn=ZnSO4+H2↑;(2)硫;(3)碳酸钠;(4)硫酸;(5)CuSO4+2NaOH=Na2SO4+Cu(OH)2↓;复分解.
点评:本题主要考查了常见物质的性质和相互转化关系.难度较大.只有熟练地掌握了常见物质的性质才能较好地完成本题.

练习册系列答案
相关题目

 (2011?湖北)甲、乙、丙、丁、戊、己是初中化学中常见的些物质,它们之间存在如下图所示的相互关系(“-”表示在一定条件下能相互反应,“→”表示在一定条件下能发生转化),己知乙是一种气体,能使澄清的石灰水变浑浊,常用丁灭火;甲、乙、丙三种物质含有一种相同的元素,且甲是一种单质;乙和丁不含相同的元素,反应①、②、③中,一个有沉淀产生,一个有气体放出,一个无明显现象.
(2011?湖北)甲、乙、丙、丁、戊、己是初中化学中常见的些物质,它们之间存在如下图所示的相互关系(“-”表示在一定条件下能相互反应,“→”表示在一定条件下能发生转化),己知乙是一种气体,能使澄清的石灰水变浑浊,常用丁灭火;甲、乙、丙三种物质含有一种相同的元素,且甲是一种单质;乙和丁不含相同的元素,反应①、②、③中,一个有沉淀产生,一个有气体放出,一个无明显现象.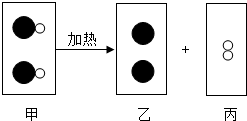 (2013?鄂尔多斯)某反应的微观示意图如图所示,其中“●”表示汞原子,“○”表示氧原子,下列说法正确的是( )
(2013?鄂尔多斯)某反应的微观示意图如图所示,其中“●”表示汞原子,“○”表示氧原子,下列说法正确的是( )