题目内容
1.在一个密闭容器中加入四种物质(无氧气),在一定条件下充分反应,测得反应前后各物质的质量如下表| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质/g | 3 | 5 | 20 | 7 |
| 反应后质量/g | 10 | 5 | 8 | 待测 |
| A. | 该反应是氧化反应 | B. | 乙物质一定是催化剂 | ||
| C. | 反应中甲、丙变化的质量比为7:8 | D. | 测得反应后丁物质的质量为12g |
分析 本题可分析先甲、乙、丙三种物质反应前后的质量变化情况,确定是反应物还是生成物;然后根据质量守恒定律确定丁是反应物还是生成物,进而可以确定反应类型.
解答 解:由表中数据分析可知,反应前后,甲的质量增加了7g,故甲是生成物,参加反应的甲的质量为7g;乙的质量不变,乙可能作该反应的催化剂,也可能没有参加反应;同理可以确定丙是反应物,参加反应的丙的质量为12g;由质量守恒定律,丁应是生成物,且生成的丁的质量为12g-7g=5g,故反应后丁物质的质量为7g+5g=12g.
A、该反应的反应物是丙,生成物是甲和丁,反应符合“一变多”的特征,属于分解反应,故选项说法错误;
B、乙的质量不变,乙可能作该反应的催化剂,也可能没有参加反应,故选项说法错误;
C、反应中甲、丙变化的质量比为:7:12,故错误;
D、由以上知,反应后丁物质的质量为7g+5g=12g,故正确.
故选D.
点评 本题难度不大,考查的是质量守恒定律的应用,解题的关键是分析表中数据,灵活运用质量守恒定律.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目
12.下列实验过程属于物理变化的是( )
| A. | 用食醋除水垢 | B. | 在蛋清溶液中滴加饱和硫酸铵溶液 | ||
| C. | 用漂白粉给河水杀菌消毒 | D. | 用葡萄酿制葡萄酒 |
9.下列物质的名称、化学式、类别都正确的是( )
| A. | 纯碱 NaHCO3 盐 | B. | 熟石灰 CaO 碱 | ||
| C. | 氧化铁 FeO 氧化物 | D. | 酒精 C2H5OH 纯净物 |
16.两种固体物质a、b的溶解度曲线如图,下列说法正确的是( )
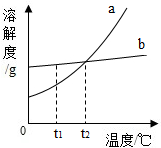

| A. | b的溶解度小于a的溶解度 | |
| B. | 在t2℃时,a、b两种固体的溶解度相等 | |
| C. | 要从b溶液中得到较多的b晶体,通常可采用降温结晶的方法 | |
| D. | 分别将t2℃时a、b两种物质的溶液降温至t1℃时,肯定都有晶体析出 |
13.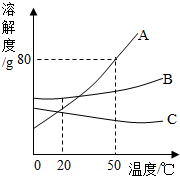 根据图的溶解度曲线判断,下列说法正确的是( )
根据图的溶解度曲线判断,下列说法正确的是( )
 根据图的溶解度曲线判断,下列说法正确的是( )
根据图的溶解度曲线判断,下列说法正确的是( )| A. | A物质的溶解度最大 | |
| B. | 升温一定能使C物质的不饱和溶液变成饱和溶液 | |
| C. | 50℃时把90gA物质放入100g水中能得到190g溶液 | |
| D. | 将50℃时三种物质的饱和溶液分别降温到20℃,B溶液的溶质质量分数最大 |
11.按下列装置进行相关实验,其中不能达到目的是( )
| A. | 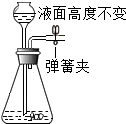 检查装置气密性 | B. | 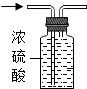 干燥O2 | C. | 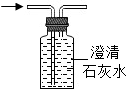 检验CO2 | D. | 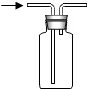 收集并储存H2 |
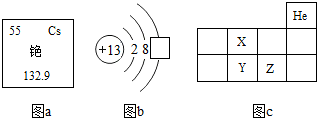 图a 是铯元素在元素周期表中的信息,图b 是铝原子结构示意图,图C 为元素周期表的一部分,X、Y、Z 代表三种不同元素.
图a 是铯元素在元素周期表中的信息,图b 是铝原子结构示意图,图C 为元素周期表的一部分,X、Y、Z 代表三种不同元素.