题目内容
绿矾(主要成分为硫酸亚铁)在工农业生产中具有重要用途:
【查阅资料】①KSCN溶液遇Fe3+变为血红色,遇Fe2+不变色;②Fe2+易被氧化为Fe3+;③SO2能使品红溶液褪色。
某化学兴趣小组同学取少量绿矾样品于试管中,加水溶解,滴加KSCN溶液,溶液颜色无明显变化,说明样品中没有___________(填离子符号),再向试管中通入氧气,观察到溶液逐渐变红。该小组同学为探究硫酸亚铁分解的产物,设计了下图所示装置进行探究:
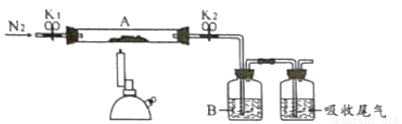
【进行实验】
(1)连接好实验仪器以后,要先______________________。
(2)装好药品后,打开K1、K2,先向装置内通入一段时间N2的原因是________________。
(3)关闭K1,点燃酒精喷灯,观察到A中固体最终变为红色粉末,B中的品红溶液褪色,说明硫酸亚铁的分解产物有____________、______________(填化学式)。若进一步实验证明分解产物中还有一种硫的氧化物,则硫酸亚铁分解的化学方程式为_________________。
Fe3+ 检查装置的气密性 排尽装置内的空气,防止硫酸亚铁被空气氧化(答案合理即可) SO2; Fe2O3; 【解析】【查阅资料】根据题中信息分析解答;【进行实验】(1)根据规范实验操作解答;(2)根据Fe2+易被氧化为Fe3+分析解答;(3)根据题中信息分析解答。【查阅资料】由题中资料可知,①KSCN溶液遇Fe3+变为血红色,遇Fe2+不变色。故某化学兴趣小组同学取少量绿矾样品于试管中,加...
练习册系列答案
相关题目
归纳总结是学习化学的重要方法,下列知识归纳正确的是
A.化学中“三” | B. 性质和用途 |
①构成物质的三种粒子:分子、原子、离子 ②三种可燃气体:氢气、甲烷、氧气 | ①碱性--用氢氧化钠改良酸性土壤 ②稳定性--用氮气填充食品包装袋 |
C.安全知识 | D.化学与生活 |
①酒精灯洒出的酒精在桌面燃烧---用湿布盖灭 ②白磷易自燃--放在冷水中密封保存 | ①去除餐具油污--用洗洁精乳化 ②硬水软化--用肥皂水 |
A. A B. B C. C D. D
C 【解析】A、②氧气不具有可燃性,错误;B、①氢氧化钠易溶于水,有强烈的腐蚀性,不能用来改良酸性土壤,错误;C、①酒精灯洒出的酒精在桌面燃烧---用湿布盖灭,②白磷易自燃--放在冷水中密封保存,正确;D、②硬水软化,实验室用蒸馏的方法,生活中用煮沸的方法,错误。故选C。


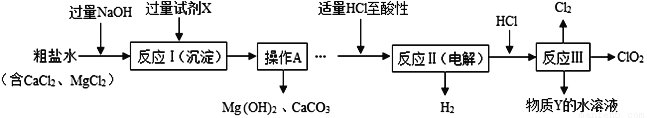 (其中反应Ⅲ制取ClO2的化学方程式为:2NaClO3+4HCl==2ClO2↑+Cl2↑+2NaCl+2H2O)
(其中反应Ⅲ制取ClO2的化学方程式为:2NaClO3+4HCl==2ClO2↑+Cl2↑+2NaCl+2H2O)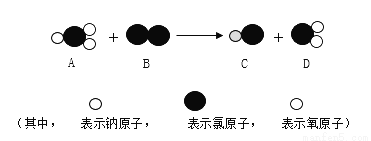
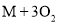

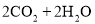 ,则M的化学式是
,则M的化学式是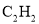 B.
B. 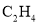 C.
C. 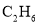 D.
D. 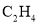 O
O