题目内容
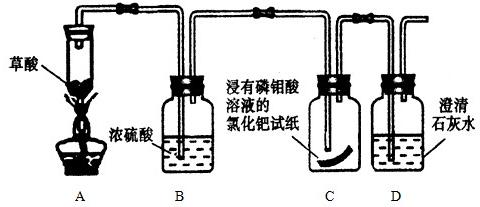
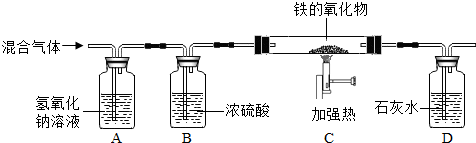
草酸加热分解产物为水、二氧化碳和一氧化碳.为了证明其生成物中一定有一氧化碳,设计了如下实验
(1)实验完毕后,测量装置A中溶液的pH______7(填“>”“=”或“<”).
(2)有同学建议将装置B中的浓硫酸改为澄清石灰水,其理由为:______.
(3)装置D中石灰水的作用是:______.
(4)在装置C中发生了化学反应,氧化铁在化学反应中做______剂.
【答案】分析:(1)根据反应后生成的溶液的成分分析,碱性溶液的pH>7判断;
(2)澄清石灰水可用来检验是否存在气体CO2;
(3)从装置特点和试剂的性质分析其作用;
(4)根据反应中失去氧是氧化剂判断.
解答:(1)实验完毕后,氢氧化钠溶液吸收二氧化碳后部分变成碳酸钠溶液,但碳酸钠溶液呈碱性,故测量装置A中溶液的pH>7.
(2)有同学建议将装置B中的浓硫酸改为澄清石灰水,这样 可以证明装置A中的NaOH溶液是否完全吸收了CO2.
(3)检验气体中含有CO的方法是检验其还原氧化铁后是否生成二氧化碳,故装置D中石灰水的作用是:能证明一氧化碳与氧化铁反应生成的CO2.
(4)在装置C中发生CO还原氧化铁的化学反应,在反应中氧化铁失去氧,在化学反应中做氧化剂.
故答案为:(1)>
(2)可以证明装置A中的NaOH溶液是否完全吸收了CO2
(3)能证明一氧化碳与氧化铁反应生成的CO2
(4)氧化
点评:验证二氧化碳将气体通过澄清石灰水,验证一氧化碳时将气体通过金属氧化物,看是否能还原出金属和生成二氧化碳.
(2)澄清石灰水可用来检验是否存在气体CO2;
(3)从装置特点和试剂的性质分析其作用;
(4)根据反应中失去氧是氧化剂判断.
解答:(1)实验完毕后,氢氧化钠溶液吸收二氧化碳后部分变成碳酸钠溶液,但碳酸钠溶液呈碱性,故测量装置A中溶液的pH>7.
(2)有同学建议将装置B中的浓硫酸改为澄清石灰水,这样 可以证明装置A中的NaOH溶液是否完全吸收了CO2.
(3)检验气体中含有CO的方法是检验其还原氧化铁后是否生成二氧化碳,故装置D中石灰水的作用是:能证明一氧化碳与氧化铁反应生成的CO2.
(4)在装置C中发生CO还原氧化铁的化学反应,在反应中氧化铁失去氧,在化学反应中做氧化剂.
故答案为:(1)>
(2)可以证明装置A中的NaOH溶液是否完全吸收了CO2
(3)能证明一氧化碳与氧化铁反应生成的CO2
(4)氧化
点评:验证二氧化碳将气体通过澄清石灰水,验证一氧化碳时将气体通过金属氧化物,看是否能还原出金属和生成二氧化碳.

练习册系列答案
相关题目