题目内容
18.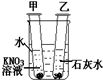 如图所示,在盛冷水烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),若使甲试管中晶体减少,乙试管中晶体增加,需向烧杯中加入的物质是( )
如图所示,在盛冷水烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),若使甲试管中晶体减少,乙试管中晶体增加,需向烧杯中加入的物质是( )| A. | 氯化钠 | B. | 硝酸钾 | C. | 硝酸铵 | D. | 氢氧化钾 |
分析 在盛冷水烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),则甲、乙两试管中的溶液分别是硝酸钾饱和溶液、氢氧化钙的饱和溶液;若使甲试管中晶体减少,乙试管中晶体增加,结合硝酸钾的溶解度随着温度的升高而增大,氢氧化钙的溶解度随着温度的升高而减小,结合常见物质溶于水的温度变化,进行分析判断.
解答 解:在盛冷水烧杯中放入甲、乙两支试管(试管中都有未溶解的该溶液的溶质),则甲、乙两试管中的溶液分别是硝酸钾饱和溶液、氢氧化钙的饱和溶液;硝酸钾的溶解度随着温度的升高而增大,氢氧化钙的溶解度随着温度的升高而减小,若使甲试管中晶体减少,乙试管中晶体增加,则应升高温度.
A、氯化钠溶于水温度几乎无变化,故选项错误.
B、硝酸钾溶于水温度几乎无变化,故选项错误.
C、硝酸铵溶于水吸热,温度降低,不符合要求,故选项错误.
D、氢氧化钾溶于水放出大量的热,温度升高,符合要求,故选项正确.
故选:D.
点评 本题难度不大,掌握结晶的原理、常见化学物质的溶解度受温度影响的变化趋势、常见物质溶于水的温度变化是正确解答本题的关键.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
6.下列性质中,不属于化学性质的是( )
| A. | 氢气具有可燃性 | B. | 铁在潮湿的空气中易生锈 | ||
| C. | 氢气比氧气密度小 | D. | 蜡烛在空气中能燃烧 |
10.在银杏果中含有银杏酸(银杏酸化学式为C22H34O3),下列有关银杏酸的说法正确的是( )
| A. | 属于氧化物 | |
| B. | 碳、氢、氧三种元素质量比是22:34:3 | |
| C. | 氢元素的质量分数最大 | |
| D. | 由三种非金属元素组成 |
7.下列有关物质的组成、结构和性质关系叙述,不正确的是( )
| A. | 保持氧气化学性质的最小微粒是氧分子 | |
| B. | 分子可分,原子不可再分 | |
| C. | 元素的化学性质与原子最外层电子数目关系密 | |
| D. | 构成物质的微粒有分子、原子、离子 |
9.从分子的角度分析,下列解释错误的是( )
| A. | 美酒飘香--分子在不断运动 | |
| B. | 热胀冷缩--分子的大小随温度的改变而改变 | |
| C. | 气态和液态的氧气都具有助燃性--分子是保持物质化学性质的最小颗粒 | |
| D. | 电解水产生氢气和氧气--分支可以分成原子,原子在重新组合成分子 |
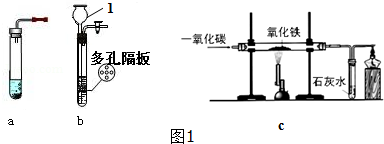 如图1所示装置制取氢气,试回答下列问题:
如图1所示装置制取氢气,试回答下列问题:
 我们已经知道.空气的主要成分是氮气和氧气.下图是测定空气中氧气含量的实验装置.试回答下列问题:
我们已经知道.空气的主要成分是氮气和氧气.下图是测定空气中氧气含量的实验装置.试回答下列问题: