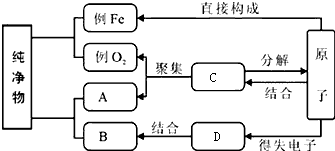
题目内容
氨气是一种无色、有刺激性气味的气体,极易溶于水,氨水显碱性.实验室用加热氯化铵和熟石灰两种固体的混合物来制取氨气,同时生成氯化钙和水.
(1)写出实验室制取氨气的化学方程式: .
(2)有下列装置如图甲:
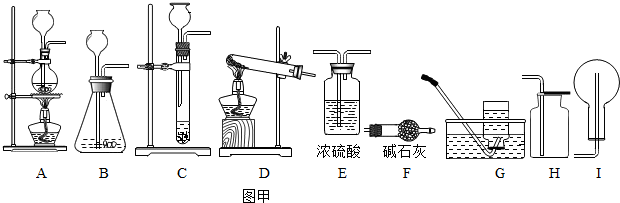
实验室制取、干燥、收集氨气的装置应分别选用(填序号) 、 、 .
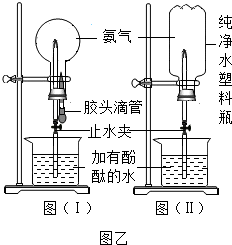
(3)按图乙(Ⅰ)连接,挤压胶头滴管使其少量的水进入烧瓶,打开止水夹,烧瓶中就可以看到 色的喷泉.按图乙(Ⅱ)连接,你怎样操作,才能引发喷泉(提示:用物理方法使氨气和烧杯中水接触可引发喷泉)
(4)实验室制取和收集CO2应选择装置 .要净化实验室制取的CO2气体,需将制得的CO2依次通过 洗气瓶、 洗气瓶.
(5)检查图甲B装置的气密性的方法是:将装置中导气管上的胶皮管用弹簧夹夹住,往长颈漏斗中注入水至液面高出锥形瓶中液面,若能观察到 现象,即可证明装置不漏气.
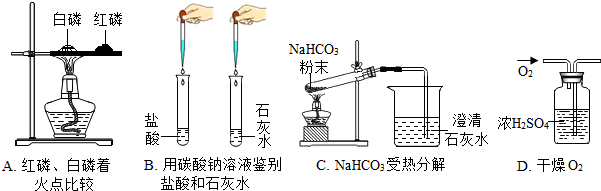
(6)用下列实验装置完成对应实验(部分仪器已省略),操作正确并能达到实验目的是 .
(1)写出实验室制取氨气的化学方程式:
(2)有下列装置如图甲:

实验室制取、干燥、收集氨气的装置应分别选用(填序号)
(3)按图乙(Ⅰ)连接,挤压胶头滴管使其少量的水进入烧瓶,打开止水夹,烧瓶中就可以看到

(4)实验室制取和收集CO2应选择装置
(5)检查图甲B装置的气密性的方法是:将装置中导气管上的胶皮管用弹簧夹夹住,往长颈漏斗中注入水至液面高出锥形瓶中液面,若能观察到
(6)用下列实验装置完成对应实验(部分仪器已省略),操作正确并能达到实验目的是

考点:常用气体的发生装置和收集装置与选取方法,检查装置的气密性,气体的干燥(除水),二氧化碳的实验室制法,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)实验室用加热氯化铵和熟石灰两种固体的混合物来制取氨气;
(2)制取气体主要看反应物的状态和反应条件;收集气体看气体的密度与水溶性;浓硫酸具有吸水性,可以做干燥剂;
(3)氨气易溶于水,故烧瓶内的氨气减少,气压减小,外界大气压压着有酚酞的水进入烧瓶;
(4)根据实验室制取二氧化碳的原理以及除去二氧化碳中氯化氢气体和水蒸气的方法分析;
(5)只要装置不漏气随着水的不断加入装置内气体的压强会不断变大达到一定压强后漏斗内液体不会下降;
(6)A、对比实验要提供相同的条件;
B、碳酸钠与盐酸反应生成二氧化碳有气泡,与石灰水反应有碳酸钙沉淀;
C、加热碳酸氢钠,产生二氧化碳可使澄清石灰水变浑浊,但加热固体时应试管略向下倾斜;
D、洗气时(干燥气体)应长管进气体,短管出气体.
(2)制取气体主要看反应物的状态和反应条件;收集气体看气体的密度与水溶性;浓硫酸具有吸水性,可以做干燥剂;
(3)氨气易溶于水,故烧瓶内的氨气减少,气压减小,外界大气压压着有酚酞的水进入烧瓶;
(4)根据实验室制取二氧化碳的原理以及除去二氧化碳中氯化氢气体和水蒸气的方法分析;
(5)只要装置不漏气随着水的不断加入装置内气体的压强会不断变大达到一定压强后漏斗内液体不会下降;
(6)A、对比实验要提供相同的条件;
B、碳酸钠与盐酸反应生成二氧化碳有气泡,与石灰水反应有碳酸钙沉淀;
C、加热碳酸氢钠,产生二氧化碳可使澄清石灰水变浑浊,但加热固体时应试管略向下倾斜;
D、洗气时(干燥气体)应长管进气体,短管出气体.
解答:解:(1)加热氯化铵和熟石灰两种固体的混合物来制取氨气,同时生成氯化钙和水.所以根据这些可以写出反应的化学方程式.
故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;
(2)加热氯化铵和熟石灰两种固体的混合物来制取氨气,故发生装置选择D;氨气属于碱性气体,可以用碱石灰干燥;氨气能溶于水,比空气的密度小,故收集装置选择I;
故答案为:D;F;I.
(3)氨气的水溶液呈碱性,能使无色的酚酞试液变红色.图Ⅱ的利用原理为:氨气溶于水后,装置内压强减小,导致外面溶液的进入,从而引发喷泉.
故答案为:红;先打开止水夹,挤压塑料瓶(或用热毛巾捂住塑料瓶),使瓶中的部分氨气溶入水中.
(4)实验室制取二氧化碳用大理石和稀盐酸,是固体和液体的不加热反应,所以用装置B做反应装置;二氧化碳的密度大于空气的密度,并且易溶于水,所以可以用向上排气法收集气体.
除去二氧化碳中的氯化氢气体应选饱和的碳酸氢钠溶液,除去其中的水蒸气,应用浓硫酸;
故答案为:BH;饱和碳酸氢钠溶液(或者硝酸银溶液);浓硫酸;
(5)只要装置不漏气随着水的不断加入装置内气体的压强会不断变大达到一定压强后漏斗内液体不会下降.
故答案为:漏斗下端有一稳定的液柱.
(6)A、白磷着火点比红磷低,应该加热二者的中间位置或同时加热(因为加热是红P,那么白P的温度一定比红P的温度低,结量一定是白P先燃烧,温度低的先燃烧,但是由于距离不确定,所以无法保证白磷先燃烧),A错误;
B、碳酸钠与盐酸有气泡,与石灰水有沉淀,现象明显,可鉴别,B正确
C、加热固体碳酸氢钠时试管口应略向下倾斜,C错误
D、干燥气体时,应长管进气体,短管出气体,D错误
故选:B.
故答案为:2NH4Cl+Ca(OH)2
| ||
(2)加热氯化铵和熟石灰两种固体的混合物来制取氨气,故发生装置选择D;氨气属于碱性气体,可以用碱石灰干燥;氨气能溶于水,比空气的密度小,故收集装置选择I;
故答案为:D;F;I.
(3)氨气的水溶液呈碱性,能使无色的酚酞试液变红色.图Ⅱ的利用原理为:氨气溶于水后,装置内压强减小,导致外面溶液的进入,从而引发喷泉.
故答案为:红;先打开止水夹,挤压塑料瓶(或用热毛巾捂住塑料瓶),使瓶中的部分氨气溶入水中.
(4)实验室制取二氧化碳用大理石和稀盐酸,是固体和液体的不加热反应,所以用装置B做反应装置;二氧化碳的密度大于空气的密度,并且易溶于水,所以可以用向上排气法收集气体.
除去二氧化碳中的氯化氢气体应选饱和的碳酸氢钠溶液,除去其中的水蒸气,应用浓硫酸;
故答案为:BH;饱和碳酸氢钠溶液(或者硝酸银溶液);浓硫酸;
(5)只要装置不漏气随着水的不断加入装置内气体的压强会不断变大达到一定压强后漏斗内液体不会下降.
故答案为:漏斗下端有一稳定的液柱.
(6)A、白磷着火点比红磷低,应该加热二者的中间位置或同时加热(因为加热是红P,那么白P的温度一定比红P的温度低,结量一定是白P先燃烧,温度低的先燃烧,但是由于距离不确定,所以无法保证白磷先燃烧),A错误;
B、碳酸钠与盐酸有气泡,与石灰水有沉淀,现象明显,可鉴别,B正确
C、加热固体碳酸氢钠时试管口应略向下倾斜,C错误
D、干燥气体时,应长管进气体,短管出气体,D错误
故选:B.
点评:本考点属于实验探究题,考查了二氧化碳与过氧化钠的有关性质和变化的规律,还考查了反应装置的选择、气体的除杂和干燥,以及化学方程式的书写,综合性比较强.既有实验过程的探究,又有结论的探究.本考点主要出现在实验题中.

练习册系列答案
相关题目
过量的红磷在100mL的空气完全燃烧,冷却到室温后,剩余气体的体积约为( )
| A、80mL | B、60mL |
| C、40mL | D、20mL |
NA表示阿伏加德罗常数的数值,下列说法中正确的是( )
| A、0.1 mol BaCl2中含Cl-数为0.1 NA |
| B、22 g CO2所含有的分子数为0.5 NA |
| C、11.2L CO2所含有的分子数为0.5 NA |
| D、常温下NA 个Cl2分子所占有的体积为22.4L |
下列实验操作中,正确的是( )
A、 |
B、 |
C、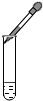 |
D、 |
在元素周期表中碳元素的信息如图所示,下列说法正确的是( )


| A、碳原子中的质子数为6 |
| B、碳属于金属元素 |
| C、碳的相对原子质量是12.01 g |
| D、碳元素只能形成一种单质 |
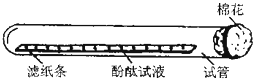 将滴有酚酞试液的滤纸条放在试管里,如图所示放在实验台上.
将滴有酚酞试液的滤纸条放在试管里,如图所示放在实验台上.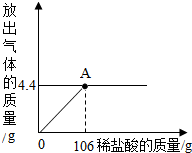 某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如右图所示,请回答:
某校化学兴趣小组为了测定某一碳酸钠样品中碳酸钠的质量分数,进行如下实验,取13.25g碳酸钠样品(杂质既不溶于酸也不溶于水)放入烧杯中,加入95.8g水使其完全溶解,再向其中加入稀盐酸,测得反应放出气体的总质量与所加入稀盐酸的质量关系曲线如右图所示,请回答: