题目内容
 人体缺锌会引起多种疾病,缺锌者可通过服用葡萄糖酸锌来补锌.如图所示是某厂生产的葡萄糖酸锌口服液的标签(部分内容不完整),请结合标签回答下列问题:
人体缺锌会引起多种疾病,缺锌者可通过服用葡萄糖酸锌来补锌.如图所示是某厂生产的葡萄糖酸锌口服液的标签(部分内容不完整),请结合标签回答下列问题:(1)葡萄糖酸锌是由
(2)葡萄糖酸锌中碳、氢、氧、锌原子的个数比是
(3)葡萄糖酸锌相对分子质量是
(4)葡萄糖酸锌中所含锌元素的质量分数是多少?(列式计算,结果保留至0.1%).
(5)已知每支口服液(20mL)含葡萄糖酸锌45.5mg,则在原图中标签“
考点:标签上标示的物质成分及其含量,化学式的书写及意义,相对分子质量的概念及其计算,元素的质量分数计算,化合物中某元素的质量计算
专题:标签图示型
分析:(1)根据葡萄糖锌的化学式即可知道它由哪几种元素组成;
(2)根据葡萄糖锌的化学式的分子构成解答;
(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;
(4)根据化合物中元素的质量分数=
计算即可;
(5)根据化合物的质量=
计算即可.
(2)根据葡萄糖锌的化学式的分子构成解答;
(3)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答;
(4)根据化合物中元素的质量分数=
| 原子的相对原子质量×原子个数 |
| 相对分子质量 |
(5)根据化合物的质量=
| 所含元素的质量 |
| 该元素的质量分数 |
解答:解:
(1)根据葡萄糖锌的化学式C12H22O14Zn可知,它由C、H、O、Zn这四种元素组成;
(2)葡萄糖酸锌中碳、氢、氧、锌原子的个数比是12:22:14:1;
(3)葡萄糖酸锌C12H22O14Zn的相对分子质量为12×12+1×22+16×14+65=455.
(4)葡萄糖酸锌中所含锌元素的质量分数为
×100%≈14.3%.
(5)45.5mg×14.3%=6.5mg,则在原图中标签含锌量上的数据应是6.5mg
答案:
(1)C、H、O、Zn四
(2)12:22:14:1
(3)455
(4)14.3%
(5)含锌量 6.5mg
(1)根据葡萄糖锌的化学式C12H22O14Zn可知,它由C、H、O、Zn这四种元素组成;
(2)葡萄糖酸锌中碳、氢、氧、锌原子的个数比是12:22:14:1;
(3)葡萄糖酸锌C12H22O14Zn的相对分子质量为12×12+1×22+16×14+65=455.
(4)葡萄糖酸锌中所含锌元素的质量分数为
| 65 |
| 455 |
(5)45.5mg×14.3%=6.5mg,则在原图中标签含锌量上的数据应是6.5mg
答案:
(1)C、H、O、Zn四
(2)12:22:14:1
(3)455
(4)14.3%
(5)含锌量 6.5mg
点评:本题主要考查学生运用质量分数公式进行计算的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列做法错误的是( )
| A、适量补钙,预防骨质疏松 |
| B、长期饮用硬水对健康有利 |
| C、食用加碘盐,预防甲状腺肿大 |
| D、推广铁强化酱油,预防缺铁性贫血 |
分析推理是化学学习中常用的思维方法.下列分析推理正确的是( )
| A、氧气和臭氧的组成元素相同,实验所以它们的化学性质相同 |
| B、离子是带电荷的微粒,所以带电荷的物质一定是离子 |
| C、明矾能与水中杂质反应,所以明矾能够净水 |
| D、二氧化锰对氰酸钾和过氧化氢的分解均有催化作用,说明同一种物质可以做不同反应的催化剂 |
下列关于水的说法错误的是( )
| A、水是人类宝贵的资源 |
| B、自然界的水都是混合物 |
| C、水能溶解很多种物质 |
| D、电解水实验能说明水由氢气和氧气组成 |
下列实验操作正确的是( )
A、 点燃酒精灯 |
B、 安装橡胶塞 |
C、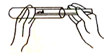 加入粉末 |
D、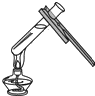 加热液体 |
规范的实验操作对于安全及实验结果来说十分重要.下列实验操作不规范的是( )
A、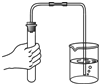 检查装置气密性 |
B、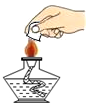 熄灭酒精灯 |
C、 给试管中液体加热 |
D、 取用液体药品 |