题目内容
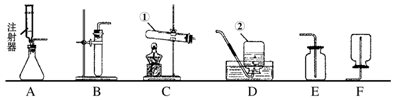
18.某纯碱样品中含有少量氯化钠杂质,现用如图所示装置来测定纯碱样品中碳酸钠的质量分数(铁架台、铁夹等在图中均已略去).
实验步骤如下:
①按图连接装置,并检查气密性;
②准确称得8g纯碱样品并放入容器B中;
③准确称得盛有碱石灰(固体氢氧化钠和生石灰的混合物)的干燥管D的质量为83.4g;
④关上K1,打开K2,缓缓滴入稀硫酸,至不再产生气泡为止;
⑤关上K2,打开K1,往试管A中缓缓鼓入空气数分钟,然后称得干燥管D的总质量为85.6g.
试回答:
(1)实验步骤⑤鼓入空气的目的是使B中产生的二氧化碳全部进入D中.
(2)若没有C装置,则会导致测定结果偏大(填“偏大”或“偏小”).
(3)根据实验中测得的有关数据,计算出纯碱样品碳酸钠的质量分数为66.25%(计算结果保留一位小数).
经精确测定,上述所求数值略大于样品中碳酸钠的实际质量分数,其原因可能是装置中有一定量的空气,所含的CO2也会进入D中.
分析 (1)根据装置的特点及实验目的,分析鼓入空气这一操作的目的;
(2)评价装置C对测定结果的影响;
(3)分析实验前后装置D质量变化,并由此质量差计算样品中碳酸钠的质量,求出样品中碳酸钠的质量分数;该装置在装药品时会不可避免的混入一些空气,据空气得出成分来分析解答.
解答 解:(1)为了减小实验误差而采取了鼓入空气的方法,把残留在装置B中二氧化碳全部由D中碱石灰吸收,实验结果更准确;
(2)浓硫酸具有吸水性,在C装置中吸收由B装置排出气体中混有的水蒸气,若少了此装置则会使气体中的水蒸气被D装置中碱石灰吸收,而使测定质量偏大;
(3)反应中放出二氧化碳气体的质量=85.6g-83.4g=2.2g
设放出2.2g二氧化碳消耗碳酸钠的质量为x
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 44
x 2.2g
$\frac{106}{x}=\frac{44}{2.2g}$
x=5.3g
所以纯碱样品Na2CO3的质量分数为:$\frac{5.3g}{8g}$×100%=66.25%;
由于在装置中不可避免的要存有残留的空气,而空气中的二氧化碳被D装置吸收,而导致测量结果偏大.
故答案为:(1)使B中产生的二氧化碳全部进入D中;
(2)偏大;
(3)66.25;装置中有一定量的空气,所含的CO2也会进入D中.
点评 本题主要考查二氧化碳和碱石灰的反应,通过本题我们要知道在完成实验时要尽可能的排除可能对实验结果产生影响的因素,例如本题中空气中二氧化碳对实验结果的影响,水蒸气的影响等.

练习册系列答案
 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
8.下列判断结果正确的是( )
(1)在一溶液中滴入石蕊溶液呈红色,溶液中无H+
(2)HCl、H2S、NH3都是非金属元素与氢的化合物,都属于无氧酸
(3)中性溶液中既没有H+也没有OH-
(4)溶液pH越大H+浓度越大,溶液的酸性越强
(5)10克10%的盐酸和10克10%的氢氧化钠溶液充分混合后,溶液呈中性,pH=7
(6)将pH=5和pH=4的溶液混合后溶液pH=9.
(1)在一溶液中滴入石蕊溶液呈红色,溶液中无H+
(2)HCl、H2S、NH3都是非金属元素与氢的化合物,都属于无氧酸
(3)中性溶液中既没有H+也没有OH-
(4)溶液pH越大H+浓度越大,溶液的酸性越强
(5)10克10%的盐酸和10克10%的氢氧化钠溶液充分混合后,溶液呈中性,pH=7
(6)将pH=5和pH=4的溶液混合后溶液pH=9.
| A. | 只有(1)(3)正确 | B. | 只有(2)(3)正确 | C. | 只有(3)(5)(6)正确 | D. | 都不正确 |
6.分类是学习和研究化学的常用方法.下列分类中正确的是( )
| A. | 有机物:甲烷、乙醇、乙酸 | |
| B. | 复合肥料:尿素[CO(NH2)2]、硝酸钾、磷酸氢二铵[NH4H2PO4] | |
| C. | 混合物:煤、石油、冰水共存物 | |
| D. | 合成材料:合金、合成橡胶、合成纤维 |
13.溶液与人类的生活息息相关,溶液的配制是日常生活中和化学实验中常见的操作,下表中是硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃).请仔细分析列式计算:
(1)取12%的硫酸溶液100毫升可配制成6%的溶液多少克
(2)向200毫升28%的氨水中加入240毫升水,摇匀,溶液的体积是多少毫升?(结果保留一位小数)
| 溶液中溶质的质量分/% | 4 | 12 | 16 | 24 | 28 |
| 硫酸溶液的密度/(g/mL) | 1.02 | 1.08 | 1.11 | 1.17 | 1.20 |
| 氨水的密度/(g/mL) | 0.98 | 0.95 | 0.94 | 0.91 | 0.90 |
(2)向200毫升28%的氨水中加入240毫升水,摇匀,溶液的体积是多少毫升?(结果保留一位小数)
10.将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各物质的质量如下.下列说法正确的是( )
| 物 质 | a | b | c | d |
| 反应前质量/g | 6.40 | 3.20 | 4.00 | 0.50 |
| 反应后质量/g | 待测 | 2.56 | 7.20 | 0.50 |
| A. | a和b是反应物,d一定是催化剂 | |
| B. | 反应后a物质的质量为4.64g | |
| C. | c物质中元素的种类,一定和a、b二种物质中元素的种类相同 | |
| D. | 若物质a与b的相对分子质量之比为2:1,则反应中a与b的化学计量数之比为4:1 |


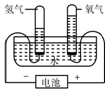 用铁片和铜片作电极通直流电使水分发现两极均产生气泡且氢气与氧气的体积比大于2:1(与理论值等于2:1不相符)实验完毕后拆下电极,发现连接电源正极(即产生氧气的一端)的金属表面颜色改变了.
用铁片和铜片作电极通直流电使水分发现两极均产生气泡且氢气与氧气的体积比大于2:1(与理论值等于2:1不相符)实验完毕后拆下电极,发现连接电源正极(即产生氧气的一端)的金属表面颜色改变了.