题目内容
下列化学反应方程式书写正确的是
A.铜加入稀盐酸中:Cu+2HCl═CuCl2+H2↑
B.二氧化碳通入足量的澄清石灰水中:CO2+Ca(OH)2═CaCO3↓+H2O
C.铁加入稀硫酸中:2Fe+3H2SO4═Fe2(SO4)3+3H2↑
D.碳酸钠固体加入稀盐酸中:Na2CO3+HCl═NaCl+H2O+CO2↑
B
【解析】
试题分析:铜加入稀盐酸中不反应,二氧化碳通入足量的澄清石灰水中:CO2+Ca(OH)2═CaCO3↓+H2O,铁加入稀硫酸中会反应生成硫酸亚铁,碳酸钠固体加入稀盐酸中:Na2CO3+HCl═NaCl+H2O+CO2↑该方程式没有配平。故选B.
考点:物质的性质和变化 化学方程式的书写

练习册系列答案
相关题目
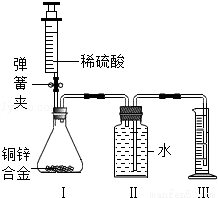
(8分)小华利用一瓶稀盐酸和相关的仪器,测定黄铜合金(Cu-Zn合金)样品的组成
(不考虑黄铜中的其他杂质)。将30mL稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 | 第二次 | 第三次 | |
连续加入盐酸的体积/mL | 10 | 10 | 10 |
生成氢气的质量/g | 0.08 | 0.08 | 0.04 |
(1)从上表数据分析,小华用10 g合金粉末总共收集到氢气_______g;
(2)求该合金中铜的质量分数。
欲除去不纯物质中的杂质(括号内为杂质),除去杂质所用方法不正确的是
选项 | 待提纯物质 | 除杂方法 |
A | O2(CO2) | 将混合气通入足量氢氧化钙溶液 |
B | CO2(CO) | 通过足量O2点燃 |
C | Cu粉(Fe粉) | 加足量稀硫酸,充分反应后过滤 |
D | N2 (O2) | 通过灼热的铜网 |