题目内容
某同学在实验室发现了一块绿色的孔雀石标本,他查阅资料知其主要成分是Cu2(OH)2CO3.他以Cu2(OH)2CO3为原料制取铜,实验流程如图(部分生成物已省略).
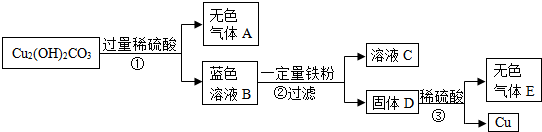
(1)溶液C中所含的溶质是 .
(2)固体D中含有的物质是 .
(3)②中反应的化学方程式: .

(1)溶液C中所含的溶质是
(2)固体D中含有的物质是
(3)②中反应的化学方程式:
考点:物质的相互转化和制备,酸的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:根据题干提供的信息结合物质的性质进行分析,碱式碳酸铜能与硫酸反应生成硫酸铜、水和二氧化碳,硫酸铜能与铁反应生成硫酸亚铁和铜,溶液C是硫酸亚铁,固体D能与硫酸反应生成无色气体E,则D中除了含有铜,还含有铁.
解答:解:(1)铁能与硫酸铜反应生成硫酸亚铁和铜,得到的固体D与硫酸反应后有气体生成,说明有铁剩余,硫酸铜全部参加反应,溶液C中只含有硫酸亚铁,故填:FeSO4;
(2)得到的固体D与硫酸反应后有气体生成,说明有铁剩余,铁与硫酸铜反应生成了铜,固体D中含有铁和铜,故填:Fe、Cu;
(3)②中反应的反应物是铁和硫酸铜,生成物是铜和硫酸亚铁,所以方程式是:Fe+CuSO4═Cu+FeSO4.
故答案为:(1)FeSO4;(2)Fe、Cu;(3)Fe+CuSO4═Cu+FeSO4.
(2)得到的固体D与硫酸反应后有气体生成,说明有铁剩余,铁与硫酸铜反应生成了铜,固体D中含有铁和铜,故填:Fe、Cu;
(3)②中反应的反应物是铁和硫酸铜,生成物是铜和硫酸亚铁,所以方程式是:Fe+CuSO4═Cu+FeSO4.
故答案为:(1)FeSO4;(2)Fe、Cu;(3)Fe+CuSO4═Cu+FeSO4.
点评:本题考查了利用碱式碳酸铜制备铜,完成此题,可以依据物质的性质进行.

练习册系列答案
相关题目
下列变化过程中,与其它三种变化不同的是( )
| A、西瓜榨成西瓜汁 |
| B、木头制成桌椅 |
| C、面皮制成面条 |
| D、糯米酿制成米酒 |
晓明在做学生实验时,将称取的a g硝酸钾晶体放入盛有b g水的烧杯中,并不断搅拌,仍有少量晶体剩余,对上述所得溶液,有关说法正确的是( )
| A、该溶液是不饱和溶液 |
| B、硝酸钾在常温时的溶解度为a g |
| C、加热该溶液,剩余晶体不会溶解 |
| D、继续加足量水可使晶体全部溶解 |
 第16届亚运会已在广州闭幕,精彩的盛会给世人留下了深刻的印象.
第16届亚运会已在广州闭幕,精彩的盛会给世人留下了深刻的印象.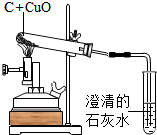 某兴趣小组同学为了探究木炭还原氧化铜所生成的气体产物是什么?
某兴趣小组同学为了探究木炭还原氧化铜所生成的气体产物是什么? 双氧水既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.小明从试剂商店购得一瓶的双氧水,用于制取氧气.其瓶上标签的部分文字如图所示,试回答下列问题:
双氧水既是工业上重要的绿色氧化剂,又是常用的医用消毒剂.小明从试剂商店购得一瓶的双氧水,用于制取氧气.其瓶上标签的部分文字如图所示,试回答下列问题: