题目内容
含磷洗涤剂因含 Na5P3OX,大量使用会造成水的污染.已知该化合物中磷元素 为+5 价,则 X 的值为( )
A. 10 B. 9 C. 7 D. 5
 A
【解析】
钠元素显+1价,磷元素的化合价为+5价,氧元素显-2价,根据在化合物中正负化合价代数和为零,可得:(+1)×5+(+5)×3+(-2)×x=0,则x=10。故选:A。
A
【解析】
钠元素显+1价,磷元素的化合价为+5价,氧元素显-2价,根据在化合物中正负化合价代数和为零,可得:(+1)×5+(+5)×3+(-2)×x=0,则x=10。故选:A。
某纯碱样品中含有少量氯化钠。现称量该样品15.4g放入烧杯中,再向其中加入一定溶质质量分数的稀盐酸至100g时恰好完全反应。此时烧杯内的物质质量为111g。试计算:
(1)碳酸钠中钠元素、碳元素、氧元素的质量比为__________;(化为最简比)
(2)反应后生成的气体质量为_________g;
(3)恰好完全反应时所得溶液中溶质的质量分数________。(计算结果精确到0.1%)
 23:6:24。。4.4;14.9%
【解析】
(1)碳酸钠化学式为Na2CO3,其中钠元素、碳元素、氧元素的质量比=23×2:12×1:16×3=23:6:24;
(2)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,根据质量守恒定律,生成二氧化碳气体的质量=15.4g+100g-111g=4.4 g;
(3)
假设样品中碳酸钠质量为x,生成的氯化钠质量为y,则有:
...
23:6:24。。4.4;14.9%
【解析】
(1)碳酸钠化学式为Na2CO3,其中钠元素、碳元素、氧元素的质量比=23×2:12×1:16×3=23:6:24;
(2)碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,根据质量守恒定律,生成二氧化碳气体的质量=15.4g+100g-111g=4.4 g;
(3)
假设样品中碳酸钠质量为x,生成的氯化钠质量为y,则有:
... 专家指出,儿童若摄入过多的反式脂肪酸将会影响身体发育。摄入蛋糕里的人造奶油可能会产生一种反式脂肪酸,其化学式是C18H34O2,下列有关该物质的说法不正确的是( )
A. C18H34O2是氧化物
B. C18H34O2是化合物
C. C18H34O2的相对分子质量为282
D. 一个C18H34O2分子由54个原子构成
 A
【解析】
A、根据氧化物是指由两种元素组成且其中一种是氧元素的化合物,进行判断可知C18H34O2不是氧化物,故A说法错误;B、化合物是由不同中元素组成的纯净物;可知C18H34O2是化合物,故B说法正确;C、根据化学式C18H34O2可知,此物质的相对分子质量=1218+134+162=282,故C说法正确;D、根据标在元素符号右下角的数字表示一个分子中所含原子的个数;可得一个C...
A
【解析】
A、根据氧化物是指由两种元素组成且其中一种是氧元素的化合物,进行判断可知C18H34O2不是氧化物,故A说法错误;B、化合物是由不同中元素组成的纯净物;可知C18H34O2是化合物,故B说法正确;C、根据化学式C18H34O2可知,此物质的相对分子质量=1218+134+162=282,故C说法正确;D、根据标在元素符号右下角的数字表示一个分子中所含原子的个数;可得一个C... 某 M 原子的实际质量为a,碳12原子的实际质量为b,则M原子的相对原子质量为( )
A.  B.
B. 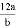 C.
C. 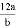 D.
D. 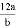 kg
kg
 B
【解析】
某M原子的实际质量为a,碳12原子的实际质量为b,则M原子的相对原子质量为=;相对原子质量单位为1,常省略不写,不是kg。故选B。
B
【解析】
某M原子的实际质量为a,碳12原子的实际质量为b,则M原子的相对原子质量为=;相对原子质量单位为1,常省略不写,不是kg。故选B。 已知A、B、C、D四种元素的化合价依次为+1、+3、﹣1、﹣2,则A、B、C、D四种元素中的某两种元素所组成的化合物的化学式不正确的是
A. AC B. AD C. A2D D. B2D3
 B
【解析】
A、A、C元素的化合价分别为+1、﹣1,则A、C元素组成的化合物的化学式为:AC;故A书写正确;
B、A、D元素的化合价分别为+1、﹣2,则A、D元素组成的化合物的化学式为:A2D;故B书写不正确;
C、A、D元素的化合价分别为+1、﹣2,则A、D元素组成的化合物的化学式为:A2D;故C书写正确;
D、B、D元素的化合价分别为+3、﹣2,则B、D元素组成...
B
【解析】
A、A、C元素的化合价分别为+1、﹣1,则A、C元素组成的化合物的化学式为:AC;故A书写正确;
B、A、D元素的化合价分别为+1、﹣2,则A、D元素组成的化合物的化学式为:A2D;故B书写不正确;
C、A、D元素的化合价分别为+1、﹣2,则A、D元素组成的化合物的化学式为:A2D;故C书写正确;
D、B、D元素的化合价分别为+3、﹣2,则B、D元素组成... 青少年过多摄入蛋糕里的人造奶油会产生一种影响身体发育的反式脂肪酸, 其化学式为 C18H34O2,下列反式脂肪酸的说法中正确的是( )
A. 该物质中 C、H、O 三种元素的质量比为 9:17:1
B. 该物质是由 18 个碳原子、34 个氢原子、2 个氧原子构成的
C. 该物质的相对分子质量为 282g
D. 该物质中质量分数最小的为氧元素
 D
【解析】
A、C18H34O2中,碳、氢、氧元素的质量比为(12×18):(1×34):(16×2)≠9:17:1,故选项错误;B、该物质是由分子构成的,而不是由原子构成的,故选项错误;C、相对分子质量的单位是“1”,通常省略,而不是“g”,故选项错误;D、反式脂肪酸中碳元素、氢元素和氧元素的质量比为12×18:34:16×2=108:17:16;可见,其中氧元素的质量分数最小,故...
D
【解析】
A、C18H34O2中,碳、氢、氧元素的质量比为(12×18):(1×34):(16×2)≠9:17:1,故选项错误;B、该物质是由分子构成的,而不是由原子构成的,故选项错误;C、相对分子质量的单位是“1”,通常省略,而不是“g”,故选项错误;D、反式脂肪酸中碳元素、氢元素和氧元素的质量比为12×18:34:16×2=108:17:16;可见,其中氧元素的质量分数最小,故... 阅读材料,回答问题。
英国化学家波义耳曾在一个敞口的容器中加热一种金属,结果发现反应后质量增加了,由此得出反应前后质量不守恒。之后俄国化学家罗蒙诺索夫在密封玻璃瓶内燃烧金属,发现反应后质量不变,由此得出反应前后质量守恒。
这两位科学家的实验相似,为何结论不同?请你和同学们一起沿着科学家的足迹进行实验探究,并完成以下相关内容:
(1)交流讨论:两位科学家得出不同的结论究竟与哪些实验因素有关呢? _____________
(2)提出假设:若用同种金属、同一容器进行实验,两位科学家得出不同的结论主要是由于_____________。
(3)实验验证:已知钠在空气中受热燃烧生成过氧化钠固体。
操作步骤及实验现象 | 简答 |
在底部铺有细沙的锥形瓶中,放入一小块金属钠,塞紧橡胶塞,称量,用砝码使天平平衡 | 称量前需 ______ |
取下锥形瓶,放在垫有石棉网的三脚架上微热,观察金属钠受热燃烧,冷却后再称量 | 称量时观察到 _____ |
将锥形瓶塞拔下一会儿后,盖上瓶塞再称量 | 称量时观察到 _____ |
(4)得出结论:假设成立。
(5)依据以上实验事实,解释两位科学家的实验结论:_______________________________________。
 可能与反应容器是否密闭有关或可能与反应物有关反应容器敞口与密闭的差异检查天平是否平衡天平保持平衡天平指针向左偏转罗蒙诺索夫在密闭容器内进行实验,金属燃烧后,质量的增加来自于瓶内空气中氧气的减少,因此反应后质量不变。波义耳在敞口容器中实验,金属燃烧消耗瓶内氧气后,瓶外的空气不断补充进入瓶内,因此反应后容器内物质质量增加
【解析】
(1)将金属放在密闭容器里煅烧,煅烧后他立即打开容器盖进行...
可能与反应容器是否密闭有关或可能与反应物有关反应容器敞口与密闭的差异检查天平是否平衡天平保持平衡天平指针向左偏转罗蒙诺索夫在密闭容器内进行实验,金属燃烧后,质量的增加来自于瓶内空气中氧气的减少,因此反应后质量不变。波义耳在敞口容器中实验,金属燃烧消耗瓶内氧气后,瓶外的空气不断补充进入瓶内,因此反应后容器内物质质量增加
【解析】
(1)将金属放在密闭容器里煅烧,煅烧后他立即打开容器盖进行... 鉴别加碘食盐的方法.向装有_____和_____混合溶液中,滴入_____, 再加入食盐,变_____,证明是加碘食盐.
 碘化钾淀粉稀 盐酸 ,蓝色
【解析】
根据题意,食盐中的碘酸钾(KIO3)在酸性条件下,可以将碘化钾(KI)变成碘(I2),碘遇淀粉变蓝色,据此进行分析解答。
食盐中的碘酸钾(KIO3)在酸性条件下,可以将碘化钾(KI)变成碘(I2),故鉴别加碘食盐的方法是向装有碘化钾和淀粉混合液的试管中,滴入稀盐酸将溶液酸化,再加入食盐,若食盐中有碘酸钾,则会生成碘,碘遇淀粉变蓝色。
碘化钾淀粉稀 盐酸 ,蓝色
【解析】
根据题意,食盐中的碘酸钾(KIO3)在酸性条件下,可以将碘化钾(KI)变成碘(I2),碘遇淀粉变蓝色,据此进行分析解答。
食盐中的碘酸钾(KIO3)在酸性条件下,可以将碘化钾(KI)变成碘(I2),故鉴别加碘食盐的方法是向装有碘化钾和淀粉混合液的试管中,滴入稀盐酸将溶液酸化,再加入食盐,若食盐中有碘酸钾,则会生成碘,碘遇淀粉变蓝色。 下列说法正确的是
A. 向酸性土壤里撒熟石灰,可调节土壤的pH
B. 推广加碘盐是为了预防胃酸过多
C. 钢铁在干燥的环境中比在潮湿的环境中更容易被腐蚀
D. 玻璃钢、光导纤维和合成纤维都是有机合成材料
 A
【解析】
试题A.向酸性土壤里撒熟石灰,可调节土壤的pH ,酸碱中和能达到目的,是正确的叙述;B.推广加碘盐是为了预防甲状腺肿大; C.钢铁在在潮湿的环境中比干燥的环境中更容易被腐蚀; D.合成纤维都是有机合成材料;玻璃钢属于复合材料;光导纤维为非金属材料;故答案选择A
A
【解析】
试题A.向酸性土壤里撒熟石灰,可调节土壤的pH ,酸碱中和能达到目的,是正确的叙述;B.推广加碘盐是为了预防甲状腺肿大; C.钢铁在在潮湿的环境中比干燥的环境中更容易被腐蚀; D.合成纤维都是有机合成材料;玻璃钢属于复合材料;光导纤维为非金属材料;故答案选择A 
