题目内容
7.三位同学在课外活动中,对同一混合某溶液进行了检验,分别得到检验的结果如表所示.阅读表格,下列说法不正确的是( )| 同学 | 溶液中检验出的物质 |
| 小明 | Na2SO4,Na2CO3 |
| 小红 | Na2SO4,BaCl2,Na2CO3 |
| 小军 | Na2SO4,NaCl,Na2CO3 |
| A. | 由于BaCl2和Na2SO4、Na2CO3均不共存,所以小红的结论一定是不正确的 | |
| B. | 小明在溶液中加入了足量的稀硝酸,其目的是检验CO32-的存在并将其除去 | |
| C. | 小明接下来在溶液中加入了足量的Ba(NO3)2溶液,用来检验是否存在SO42-,并将产生的沉淀完全过滤 | |
| D. | 小军同学在被测溶液中加入了足量的BaCl2溶液,过滤后在滤液中加入硝酸银溶液后发现有白色沉淀,说明原溶液中含Cl-,则小明的结论也是错误的 |
分析 根据各种物质在溶液中能否共存及在检验氯离子时,我们可用硝酸银和稀硝酸;在检验硫酸根离子时,我们可用硝酸钡和稀硝酸;为了排除碳酸根离子的干扰,我们可以先加硝酸排除碳酸根离子的干扰等进行分析.
解答 解:A、BaCl2和Na2SO4、Na2CO3能够反应产生沉淀,均不共存,因此小红的结论一定是不正确的,故说法正确;
B、为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子,要确定氯离子和硫酸根离子,必须排除碳酸根离子的干扰,所以首先应检验并除去碳酸根离子.所以可先加过量的硝酸,观察是否有气体生成,检验并除去碳酸根离子,故说法正确;
C、因为硝酸钡和硫酸根离子结合产生硫酸钡沉淀,因此在溶液中加入了足量的Ba(NO3)2溶液,用来检验是否存在SO42-,故说法正确;
D、加入氯化钡会引入氯离子,和硝酸银反应产生沉淀,因此不能确定原溶液中是否含有氯离子,故说法错误;
故选项为:D.
点评 本题主要考查了溶液中的离子的检验和共存问题,在确定溶液的组成时,首先要保证所确定的溶液中的溶质必须保证能在同一溶液中共存,也就是所确定的溶质不能发生化学反应,注意溶质能在同一溶液中共存是指溶质不能发生化学反应是解答的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列药品与水接触后,温度降低的是( )
| A. | 烧碱 | B. | 硝酸铵 | C. | 浓硫酸 | D. | 氯化钠 |
19.常温下,饱和石灰水的pH约为11.3,现往一定量饱和石灰水中加入下列固体物质,恢复到常温时,溶液的pH一定不会发生改变的是( )
| A. | NaOH | B. | MgCl2 | C. | Na2CO3 | D. | CaO |
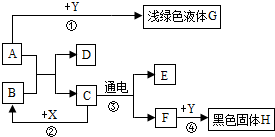 如图所示,A~H是初中化学常见的物质,A和B可发生中和反应,C为生活中最常见的液体,F可供给呼吸,X常用作食品干燥剂,Y为单质,请根据图示回答下列问题:
如图所示,A~H是初中化学常见的物质,A和B可发生中和反应,C为生活中最常见的液体,F可供给呼吸,X常用作食品干燥剂,Y为单质,请根据图示回答下列问题: