题目内容
铁及其化合物在生产生活中应用广泛。
(一)铁的化合物制备
用废铁屑制备铁红( 主要成分为 Fe2O3)和 K2SO4 的部分流程如下图所示:
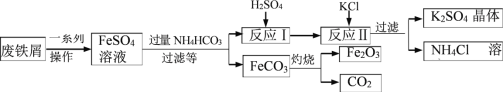
(1)加过量 NH4HCO3 反应时温度不宜过高的原因为 _____。
(2)反应Ⅰ生成的气体化学式是 _____;K2SO4 和 NH4Cl 在农业生产中都可做 _____。
(3)为检验 K2SO4 中是否混有 Cl-,要先加入足量 _____溶液,静置后再加向上层清液中滴加少量 _____溶液。
(4)在空气中灼烧 FeCO3 的化学方程式为 _____。
(二)铁的冶炼和探究
取 29.0g Fe2O3 粉末,小组同学用下图装置模拟炼铁,并测定反应后固体成分。

资料:碱石灰可吸收 H2O 和 CO2。
(1)连接装置,先______,再装入药品。
(2)实验时先通入 CO,目的是______。
(3)通过测定装置B 中固体质量变化情况,可求得A 中剩余固体质量,装置C 的作用是______。
(4)现直接测得装置A 中剩余固体质量为 21.0g,则装置 B 中固体应增重______g。
某兴趣同学在实验室的试剂柜中发现一瓶失去标签的无色溶液,可能是硫酸、硝酸铜、氯化钠、氢氧化钡中的其中一种。为了确定该无色溶液并预测其化学性质,进行下列实验:
(1)根据上述信息判断,该溶液一定不是____溶液。(填化学式,下同)
(2)取样,用pH试纸测定该溶液呈碱性,该溶液一定是_____溶液。
(3)请预测其化学性质,说出预测依据,并设计实验验证。
限用试剂:酚酞溶液、铁、盐酸、氧化铜、硫酸钾溶液、硝酸钾溶液、硝酸铜溶液。
预测 | 预测的依据 | 检验预测的实验操作与预测现象 |
①能与含有SO42-的盐反应 | ____ | 取少量待测溶液于试管中,滴入溶液,如果观察到则预测成立。 |
②能与___(填物质类别)反应 | ____ | 取少量待测溶液于试管中,_,如果观察到__,则预测成立。 |
③能与___(填物质类别)反应 | ____ | 取少量待测溶液于试管中,_,如果观察到__,则预测成立。 |
④能与___(填物质类别)反应 | ___ | 取少量待测溶液于试管中,__,如果观察到_,则预测成立。 |
下列实验操作能达成实验目的是
选项 | 实验目的 | 实验操作 |
A | 比较合金与纯金属的硬度 | 用黄铜片和纯铜片相互刻划 |
B | 检验CO2是否集满 | 向集气瓶中加入澄清石灰水,振荡 |
C | 验证质量守恒定律 | 称量镁条在空气中点燃前、后固体的质量 |
D | 证明CO2能与水反应 | 向盛满CO2的塑料瓶中倒水,拧紧瓶盖并振荡 |
A. A B. B C. C D. D
在一个密闭容器中有X、Y、Z、Q四种物质,一定条件下充分反应,测得反应前后各物质的质量如表所示:
X | Y | Z | Q | |
反应前的质量/g | 8 | 10 | 1 | 21 |
反应后的质量/g | 0 | 21 | 待测 | 9 |
已知X和Q两种物质的相对分子质量均为M,下列推理中正确的是( )
A. 反应后物质Z的质量为9g
B. 该反应是分解反应
C. 反应中物质Y与Q发生改变的质量之比为1:1
D. 该反应的化学方程式中,物质X与Q的化学计量数之比为2:3




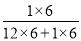 ×100%
×100%