题目内容
有一包白色粉末,可能含有K2SO4、Na2CO3、BaCl2、CuSO4中的一种或几种。取样溶于足量的水,有白色沉淀产生,过滤,滤液呈无色;向沉淀中滴加稀盐酸,产生沉淀的质量与加入盐酸体积的关系如图所示。由此推断白色粉末的成分是( )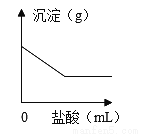
A. 可能有 BaCl2 B. 可能有Na2SO4
C. 肯定只有Na2CO3 D. 肯定有K2SO4、Na2CO3、BaCl2,没有CuSO4
D 【解析】图象中沉淀的量先是下降然后不变,说明生成的沉淀中既有能与盐酸反应的碳酸钡(碳酸钠和氯化钡反应得到)又有不能溶于盐酸的硫酸钡(硫酸钾和氯化钡反应生成的),由于过滤,滤液呈无色,所以固体中不可能含有硫酸铜(硫酸铜的溶液呈蓝色)所以白色固体中一定含有硫酸钾、碳酸钠和氯化钡,一定不含硫酸铜。故选D。
练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目