题目内容
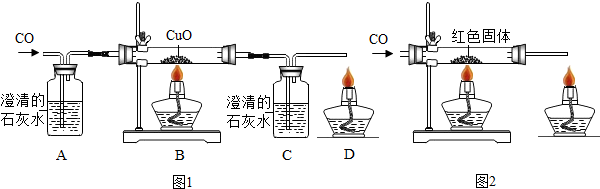
3.有一混合气体N2、CO、H2、CO2一次通过澄清石灰水、灼热的氧化铜、浓硫酸(吸水、作干燥剂),假设每步反应都很彻底.剩余气体有N2、CO2.分析 根据二氧化碳能与澄清石灰水反应,氢气和一氧化碳能与灼热的氧化铜反应,浓硫酸具有吸水性,据此进行分析判断即可.
解答 解:混合气体通过澄清石灰水后,二氧化碳会与石灰水中的氢氧化钙反应生成碳酸钙和水,CO2被吸收;再通过灼热的氧化铜后,一氧化碳和氢气具有还原性,会与灼热的氧化铜反应分别生成铜和二氧化碳、铜和水,一氧化碳和氢气被吸收,但生成了二氧化碳和水蒸气;再通过浓硫酸除去水蒸气,最后剩余的气体为二氧化碳和氮气.
故答案是:N2、CO2.
点评 本题难度不是很大,熟练掌握常见气体的性质是正确解答此类题的关键;解题时要注意在反应中是否生成了新的气体,从而准确判断最后得到的气体.

练习册系列答案
 名题金卷系列答案
名题金卷系列答案
相关题目
14.向100g稀硫酸中加入13g的锌粒完全反应后所得溶液中溶质的质量分数是( )
| A. | 13% | B. | 11.5% | C. | 19.6% | D. | 28.6% |
11.解决环境问题需要科技进步,如CO2含量不断升高,使全球气候问题日趋严重,科学家认为,人类不仅要努力减少CO2的排放,更重要的是将CO2转化为有用物质,如将C02转化为化工原料乙烯(C2H4),其反应的微观过程如图所示:

下列说法不正确的是( )

下列说法不正确的是( )
| A. | 该反应若能广泛应用,将有助于缓解温室效应 | |
| B. | 反应前后氧元素的化合价不变 | |
| C. | 该反应生成了三种物质 | |
| D. | 每2个CO2分子与8个H2分子恰好完全反应 |
15.下列物质中属于酸式盐的是( )
| A. | K2CO3 | B. | NH4Cl | C. | NaHSO4 | D. | BaSO4 |
17.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如表.下列说法中正确的是.
A.该反应为化合反应 B.甲、乙两种物质间参加反应的质量比为1:4
C.丙可能为该反应的催化剂 D.乙、丁两种物质间反应的质量比为7:5.
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质质量/g | 8 | 32 | 5 | 4 |
| 反应后物质质量/g | 16 | 4 | x | 24 |
C.丙可能为该反应的催化剂 D.乙、丁两种物质间反应的质量比为7:5.
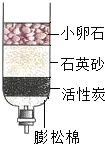 如图是某同学制作的简易净水器,请回答下列有关问题:
如图是某同学制作的简易净水器,请回答下列有关问题: