题目内容
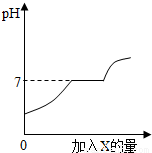
现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示。则X是

A.水
B.澄清石灰水
C.纯碱溶液
D.稀盐酸
【答案】
C
【解析】盐酸和CaCl2的混合溶液显酸性,加入显中性或显酸性的物质时,溶液的pH不可能等于或大于7;加入显碱性的溶液时,溶液的pH可能等于或大于7.
A、向盐酸和CaCl2的混合溶液中加入水时,溶液的pH升高,但是溶液的pH不可能等于或大于7.错误;
B、向盐酸和CaCl2的混合溶液中加入石灰水时,盐酸和氢氧化钙反应生成氯化钙和水,当盐酸和氢氧化钙恰好完全反应时,溶液显中性,pH等于7,继续加入石灰水时,因为石灰水显碱性,随着氢氧化钙的加入,氢氧化钙的浓度慢慢越来越高,所以溶液的pH升高,而不会出现中pH保持不变的一段.错误.;
C、向盐酸和CaCl2的混合溶液中加入碳酸钠溶液时,碳酸钠和盐酸反应,当碳酸钠和盐酸恰好完全反应时,溶液显中性,pH等于7,继续加入碳酸钠溶液时,碳酸钠和氯化钙反应生成碳酸钙和氯化钠,当碳酸钠和氯化钙恰好完全反应时,溶液的pH仍然等于7,继续加入碳酸钠溶液时,因为碳酸钠溶液显碱性,所以溶液的pH升高.正确;
D、向盐酸和CaCl2的混合溶液中加入稀盐酸时,溶液的pH不可能等于或大于7.错误
故选C

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目

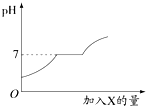 23、现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如右图所示.则X是( )
23、现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如右图所示.则X是( ) (2012?工业园区模拟)现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )
(2012?工业园区模拟)现有盐酸和CaCl2的混合溶液,向其中逐滴加入过量某物质X,溶液的pH随滴入X的量的变化关系如图所示.则X是( )