题目内容
20.下面是几种粒子的结构示意图: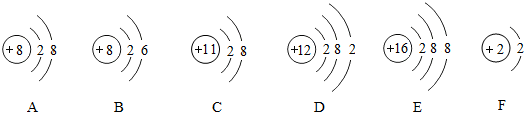
(1)A~F共有5种元素,属于非金属元素的是ABE,B所表示的元素位于元素周期表的第二周期,该元素的原子容易得到(填“得到”或“失去”)电子.Na+的结构示意图是图中的C (填字母).
(2)表示原子的粒子有BDF(填序号,下同);
(3)表示阴离子的有AE;
(4)表示阳离子的有C;
(5)表示相对稳定结构的是ACEF;
(6)在化学反应中易失去电子的粒子是D.
(7)硫元素的化学性质与B相似.
(8)氯原子的核电荷数是17;钠原子与氯原子的最本质区别是质子数不同.
分析 (1)根据质子数相同的为同一种元素进行解答;
(2)根据原子中质子数等于电子数进行解答;
(3)根据阴离子中质子数小于核外电子数进行解答;
(4)根据阳离子中质子数大于核外电子数进行解答;
(5)根据微粒的最外层电子数为8(氦为2)属于稳定结构进行解答;
(6)根据最外层电子数小于4,在化学反应中易失去电子进行解答;
(7)根据最外层电子数相同化学性质相似进行解答;
(8)根据钠原子与氯原子的最本质区别是质子数不同进行解答.
解答 解:(1)A~F共有5种质子数,共有5种元素,属于非金属元素的是ABE,B所表示的元素原子核外存在2个电子层,所以位于元素周期表的第二周期;该原子最外层有6个电子易得到电子达到稳定结构.钠离子是失去1个电子后形成的,所以Na+的结构示意图是图中的C;故填:5;ABE;二;得到;C;
(2)B中质子数等于核外电子数=8,D中质子数等于核外电子数=12,F中质子数等于核外电子数=2,属于原子;故填:BDF;
(3)阴离子中质子数小于核外电子数,AE中质子数<核外电子数,为阴离子;故填:AE;
(4)阳离子中质子数大于核外电子数,C中质子数>核外电子数,为阳离子;故填:C;
(5)ACEF最外层电子数排满了,故ACEF表示相对稳定结构;故填:ACEF;
(6)D最外层电子数小于4,在化学反应中易失去电子;故填:D;
(7)B最外层电子数与硫原子的最外层电子数为6,所以化学性质相似;故填:B;
(8)氯原子的核电荷数是17,钠原子与氯原子的最本质区别是质子数不同.故填:17;质子数不同.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,了解粒子结构示意图的意义是正确解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
15.下列有关氧气的叙述正确的是( )
| A. | 铁丝在氧气中燃烧,发出耀眼的白光,生成黑色固体 | |
| B. | 空气中氧气含量的测定实验中,可以将铜丝换成木炭 | |
| C. | 用含有氧元素的物质反应才有可能产生氧气 | |
| D. | 电解水时正极产生的气体比负极产生的气体多 |
8.将燃着的木条伸入集气瓶中,木条立即熄灭,则瓶内的气体一定不可能的是( )
| A. | 氮气 | B. | 二氧化碳 | C. | 氧气 | D. | 稀有气体 |
5.探究题一稀盐酸溶液中哪一种粒子(H2O、Cl-、H+)能是指示剂变色.
实验步骤:(1)在第一只试管中加入月2毫升蒸馏水,滴入几滴紫色石蕊溶液,观现象.
(2)在第二支试管加入约2毫升NaCl溶液滴入几滴紫色石蕊溶液,观察现象
(3)在第三支试管中加入约2毫升稀盐酸溶液,滴入几滴紫色石蕊溶液,观现象
实验1现象:没变色,你得出结论是H2O不能使石蕊变色.
实验2现象没变色,说明Cl-不能使石蕊变色
实验3现象变红,你得出结论是H+使石蕊变色
探究二探究酸和碱能否发生反应
梦阳向试管中加入2毫升NaOH溶液,滴入几滴酚酞溶液,溶液显红色,然后她又用滴管连续滴入一定量的稀硫酸,溶液有红色为无色,说明酸和将能发生反应2NaOH+H2SO4=Na2SO4+2H2O(反应方程式),大家对梦阳得到的无色溶液继续探究.李阳认为恰好中和,反应后溶液中的溶质只有Na2SO4,你认为对吗?不对,原因如果硫酸滴加过量,反应后的溶液呈酸性,酚酞也会呈无色.同学们根据以下2种方案进行实验后,反应后溶液中的溶质有2种Na2SO4、H2SO4,请你补填下表的空缺.
结论:酸和碱可以发生反应,反应的微观实质H++OH-=H2O.
探究三.熟石灰变质的探究
熟石灰露置在空气中,得到的白色固体可能是Ca(OH)2,也可能是CaCO3,你认为白色固体可能是Ca(OH)2、CaCO3.请你设计实验证明你的猜想(填下表)
根据(1)(2)现象确定你的猜想白色固体是Ca(OH)2、CaCO3是正确的.
实验步骤:(1)在第一只试管中加入月2毫升蒸馏水,滴入几滴紫色石蕊溶液,观现象.
(2)在第二支试管加入约2毫升NaCl溶液滴入几滴紫色石蕊溶液,观察现象
(3)在第三支试管中加入约2毫升稀盐酸溶液,滴入几滴紫色石蕊溶液,观现象
实验1现象:没变色,你得出结论是H2O不能使石蕊变色.
实验2现象没变色,说明Cl-不能使石蕊变色
实验3现象变红,你得出结论是H+使石蕊变色
探究二探究酸和碱能否发生反应
梦阳向试管中加入2毫升NaOH溶液,滴入几滴酚酞溶液,溶液显红色,然后她又用滴管连续滴入一定量的稀硫酸,溶液有红色为无色,说明酸和将能发生反应2NaOH+H2SO4=Na2SO4+2H2O(反应方程式),大家对梦阳得到的无色溶液继续探究.李阳认为恰好中和,反应后溶液中的溶质只有Na2SO4,你认为对吗?不对,原因如果硫酸滴加过量,反应后的溶液呈酸性,酚酞也会呈无色.同学们根据以下2种方案进行实验后,反应后溶液中的溶质有2种Na2SO4、H2SO4,请你补填下表的空缺.
| 操作 | 现象 | 结论 |
| 方案1:取少许反应后溶液置于试管中,向其中加入石蕊试液 | 溶液显红色 | 有2种溶质 |
| 方案2:取少许反应后的溶液置于试管中,向其中加入锌 | 产生气泡 | 有2种溶质 |
探究三.熟石灰变质的探究
熟石灰露置在空气中,得到的白色固体可能是Ca(OH)2,也可能是CaCO3,你认为白色固体可能是Ca(OH)2、CaCO3.请你设计实验证明你的猜想(填下表)
| (1)取固体加入水中过滤,滤液滴加酚酞溶液 | 滤液变红,说明固体中有氢氧化钙 |
| (2)滤渣加盐酸观察 | 滤渣有气泡,说明固体中有碳酸钙. |
12.2016年5月份以来,我县连续干旱,终于在9月20日下了一场大雨,大雨过后我们会觉得空气清新,碧空如洗.这主要是因为( )
| A. | 气温大幅度下降 | B. | 空气中颗粒物大量减少 | ||
| C. | 空气中氧气含量增加 | D. | 空气中二氧化碳含量增加 |
9.下列反应属于氧化反应,但不属于化合反应的是( )
| A. | 高锰酸钾受热分解 | |
| B. | 硫在氧气中燃烧 | |
| C. | 氢气在氧气中燃烧生成 水 | |
| D. | 酒精在氧气中燃烧生成水和二氧化碳 |
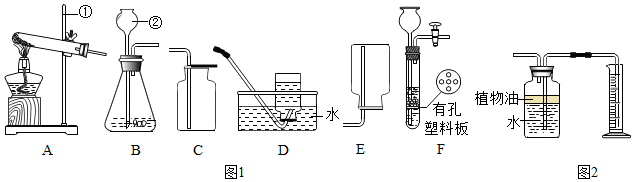
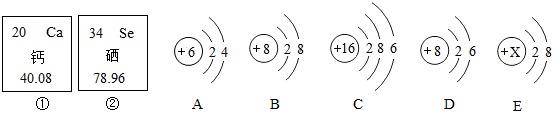
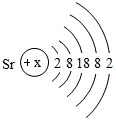 则x=38.锶元素应位于元素周期表第五周期.
则x=38.锶元素应位于元素周期表第五周期.