题目内容
 硝酸钾的溶解度曲线和相关实验如下:
硝酸钾的溶解度曲线和相关实验如下:
| 步骤 | 实验操作 |
| Ⅰ | 取100g水加入20g硝酸钾搅拌,恢复至20℃ |
| Ⅱ | 再加11.6g硝酸钾,搅拌,恢复至20℃ |
| Ⅲ | 再加20g硝酸钾,搅拌,恢复至20℃ |
| Ⅳ | 加热至固体完全溶解 |
| Ⅴ | 冷却至20℃ |
①从溶解度曲线可知:硝酸钾溶解度随着温度升高而________(增大、减小、不变).
②步骤Ⅰ~Ⅴ实验操作后均可以得到溶液,其中一定属于不饱和溶液的是________
(填:步骤序号,下同),溶质质量分数一定相等的是________;
③步骤Ⅴ冷却至20℃,析出晶体的质量为(选填字母)________
A.20g B.31.6g C.51.6g.
增大 Ⅰ Ⅱ、Ⅲ、Ⅴ A
分析:①由溶解度曲线图考虑即可;②根据20℃硝酸钾的溶解度和溶质质量分数的计算考虑;③根据溶液中溶质的质量与20℃硝酸钾的溶解度数值的差值考虑.
解答:①由溶解度曲线图可知硝酸钾溶解度随着温度升高而增大;
②20℃硝酸钾的溶解度是31.6g,所以100g水中最多溶解31.6g硝酸钾,步骤Ⅰ中100g水中加入20g,没有达到饱和,溶质质量分数为: ×100%=16.7%;步骤Ⅱ中又加入11.6g,溶质变成了31.6g,刚好达到饱和,溶质质量分数:
×100%=16.7%;步骤Ⅱ中又加入11.6g,溶质变成了31.6g,刚好达到饱和,溶质质量分数: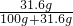 ×100%=24%;步骤Ⅲ中再加20g硝酸钾,搅拌,恢复至20℃,溶液没有将20g硝酸钾溶解,溶液已经达到饱和了,溶质质量分数:
×100%=24%;步骤Ⅲ中再加20g硝酸钾,搅拌,恢复至20℃,溶液没有将20g硝酸钾溶解,溶液已经达到饱和了,溶质质量分数: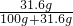 ×100%=24%;步骤Ⅳ中加热至固体完全溶解,溶液可能刚好饱和,也可能不饱和,溶质质量分数:
×100%=24%;步骤Ⅳ中加热至固体完全溶解,溶液可能刚好饱和,也可能不饱和,溶质质量分数: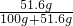 ×100%=34%;步骤Ⅴ冷却至20℃,会析出晶体,溶液是饱和溶液,溶质质量分数:
×100%=34%;步骤Ⅴ冷却至20℃,会析出晶体,溶液是饱和溶液,溶质质量分数: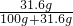 ×100%=24%;所以不饱和溶液是Ⅰ;溶质质量分数一定相等的是Ⅱ、Ⅲ、Ⅴ;
×100%=24%;所以不饱和溶液是Ⅰ;溶质质量分数一定相等的是Ⅱ、Ⅲ、Ⅴ;
③步骤Ⅴ冷却至20℃,析出晶体的质量为:51.6g-31.6g=20g,故选A.
故答案为:①增大;②Ⅰ;Ⅱ、Ⅲ、Ⅴ;③A.
点评:解答本题关键是要知道溶解度曲线表示的意义,知道利用溶解度判断溶液是否饱和的方法,熟悉溶质质量分数的计算方法.
分析:①由溶解度曲线图考虑即可;②根据20℃硝酸钾的溶解度和溶质质量分数的计算考虑;③根据溶液中溶质的质量与20℃硝酸钾的溶解度数值的差值考虑.
解答:①由溶解度曲线图可知硝酸钾溶解度随着温度升高而增大;
②20℃硝酸钾的溶解度是31.6g,所以100g水中最多溶解31.6g硝酸钾,步骤Ⅰ中100g水中加入20g,没有达到饱和,溶质质量分数为:
 ×100%=16.7%;步骤Ⅱ中又加入11.6g,溶质变成了31.6g,刚好达到饱和,溶质质量分数:
×100%=16.7%;步骤Ⅱ中又加入11.6g,溶质变成了31.6g,刚好达到饱和,溶质质量分数: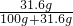 ×100%=24%;步骤Ⅲ中再加20g硝酸钾,搅拌,恢复至20℃,溶液没有将20g硝酸钾溶解,溶液已经达到饱和了,溶质质量分数:
×100%=24%;步骤Ⅲ中再加20g硝酸钾,搅拌,恢复至20℃,溶液没有将20g硝酸钾溶解,溶液已经达到饱和了,溶质质量分数: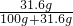 ×100%=24%;步骤Ⅳ中加热至固体完全溶解,溶液可能刚好饱和,也可能不饱和,溶质质量分数:
×100%=24%;步骤Ⅳ中加热至固体完全溶解,溶液可能刚好饱和,也可能不饱和,溶质质量分数: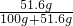 ×100%=34%;步骤Ⅴ冷却至20℃,会析出晶体,溶液是饱和溶液,溶质质量分数:
×100%=34%;步骤Ⅴ冷却至20℃,会析出晶体,溶液是饱和溶液,溶质质量分数: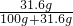 ×100%=24%;所以不饱和溶液是Ⅰ;溶质质量分数一定相等的是Ⅱ、Ⅲ、Ⅴ;
×100%=24%;所以不饱和溶液是Ⅰ;溶质质量分数一定相等的是Ⅱ、Ⅲ、Ⅴ;③步骤Ⅴ冷却至20℃,析出晶体的质量为:51.6g-31.6g=20g,故选A.
故答案为:①增大;②Ⅰ;Ⅱ、Ⅲ、Ⅴ;③A.
点评:解答本题关键是要知道溶解度曲线表示的意义,知道利用溶解度判断溶液是否饱和的方法,熟悉溶质质量分数的计算方法.

练习册系列答案
相关题目
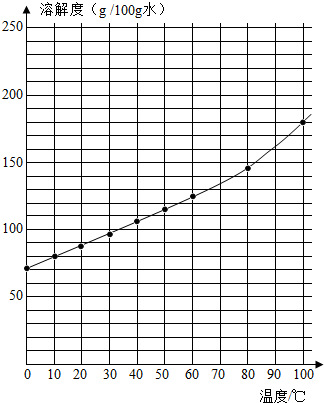
(1)如图是一张绘制到一半的溶解度曲线图,其中只有硝酸钠的溶解度曲线,请根据表格在图中继续画出硝酸钾的溶解度曲线.
 (2)根据溶解度曲线,小李设计了如下实验:
(2)根据溶解度曲线,小李设计了如下实验:
A、B两个烧杯中分别加入10克硝酸钾和硝酸钠,然后分别加入20mL水,在室温(20℃)下,烧杯A中固体全部溶解,烧杯B中尚有固体未溶解.则烧杯A中溶液的质量百分比浓度为 (保留一位小数),烧杯B中所形成的是 (填“悬浊液”、“乳浊液”或“溶液”),如果将烧杯B中不溶的固体过滤之后,剩余溶液是否饱和 (填“是”或“否”);烧杯B中还未溶解的物质为 ,由此可鉴别出硝酸钾和硝酸钠.
| 温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 溶解度(g/100g水) | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 |
 (2)根据溶解度曲线,小李设计了如下实验:
(2)根据溶解度曲线,小李设计了如下实验:A、B两个烧杯中分别加入10克硝酸钾和硝酸钠,然后分别加入20mL水,在室温(20℃)下,烧杯A中固体全部溶解,烧杯B中尚有固体未溶解.则烧杯A中溶液的质量百分比浓度为
 硝酸钾的溶解度曲线和相关实验如下:
硝酸钾的溶解度曲线和相关实验如下:| 步骤 | 实验操作 |
| Ⅰ | 取100g水加入20g硝酸钾搅拌,恢复至20℃ |
| Ⅱ | 再加11.6g硝酸钾,搅拌,恢复至20℃ |
| Ⅲ | 再加20g硝酸钾,搅拌,恢复至20℃ |
| Ⅳ | 加热至固体完全溶解 |
| Ⅴ | 冷却至20℃ |
①从溶解度曲线可知:硝酸钾溶解度随着温度升高而 (增大、减小、不变).
②步骤Ⅰ~Ⅴ实验操作后均可以得到溶液,其中一定属于不饱和溶液的是
(填:步骤序号,下同),溶质质量分数一定相等的是 ;
③步骤Ⅴ冷却至20℃,析出晶体的质量为(选填字母)
A.20g B.31.6g C.51.6g.
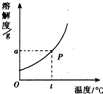 20、小明准备绘制硝酸钾和熟石灰的溶解度曲线,但他只完成了其中一种物质的溶解度曲线(如图),小明绘制的是
20、小明准备绘制硝酸钾和熟石灰的溶解度曲线,但他只完成了其中一种物质的溶解度曲线(如图),小明绘制的是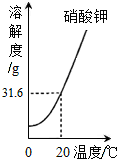 (2013?青浦区二模)硝酸钾的溶解度曲线和相关实验如下:
(2013?青浦区二模)硝酸钾的溶解度曲线和相关实验如下: