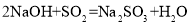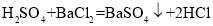题目内容
某化工厂排出的废水透明、澄清、略显蓝色。某同学取少量废水,用盐酸酸化,有白色沉淀生成(不溶于稀硝酸)。过滤,将所得的滤液分成两份,一份滤液中加入稀硫酸,也有白色沉淀生成(不溶于稀硝酸);另一份滤液中加入足量NaOH溶液,产生蓝色沉淀。已知白色的Fe(OH)2固体在潮湿的空气中可生成红褐色的Fe(OH)3。试回答:
(1)废水中一定含有的酸根离子是______(填字母)
A C1- B NO3- C CO32- D SO42-
(2)过滤后,向滤液中滴加NaOH溶液,开始时观察不到蓝色沉淀,原因是:_____。
(3)该同学设计了一个从废水中除去重金属离子的实验方案如下:

①固体A中一定含有的物质为_____(写化学式)。
②你认为金属X、Ba的活动性强弱关系是:X______Ba(填“>”“<”或“=”)。
③反应(Ⅲ)的化学方程式为_______。
练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目