题目内容
18.食盐是一种重要的化工原料,由于粗盐中含有少量泥沙和MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如图,请回答下列问题:
(1)操作Ⅱ所用的玻璃仪器有什么?
(2)如何判定操作Ⅲ加入盐酸达到适量?
(3)请写出在操作I的悬浊液中加入Na2CO3溶液的作用Na2CO3+BaCl2=BaCO3↓+2NaCl、Na2CO3+CaCl2=CaCO3↓+2NaCl(用化学方程式表示).
分析 (1)根据经过操作Ⅱ后,得到了沉淀和滤液,所以操作Ⅱ是过滤,在过滤操作中用到的玻璃仪器有烧杯、漏斗、玻璃棒进行分析;
(2)根据碳酸钠和盐酸反应会生成二氧化碳气体进行分析;
(3)根据碳酸钠和氯化钡反应会生成碳酸钡沉淀和氯化钠、氯化钙和碳酸钠反应会生成碳酸钙沉淀和氯化钠进行分析.
解答 解:(1)经过操作Ⅱ后,得到了沉淀和滤液,所以操作Ⅱ是过滤,在过滤操作中用到的玻璃仪器有烧杯、漏斗、玻璃棒;
(2)碳酸钠和盐酸反应会生成二氧化碳气体,所以判定操作Ⅲ加入盐酸达到适量的方法是:滴加盐酸至溶液恰好没有气泡产生;
(3)碳酸钠和氯化钡反应会生成碳酸钡沉淀和氯化钠、氯化钙和碳酸钠反应会生成碳酸钙沉淀和氯化钠,化学方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl、Na2CO3+CaCl2=CaCO3↓+2NaCl.
故答案为:(1)烧杯、漏斗、玻璃棒;
(2)滴加盐酸至溶液恰好没有气泡产生;
(3)Na2CO3+BaCl2=BaCO3↓+2NaCl、Na2CO3+CaCl2=CaCO3↓+2NaCl.
点评 本题主要考查了粗盐提纯时的物质的除杂和净化,在除杂质时不要引入新的杂质,了解混合物的分离和除杂的方法是解答本题的基础知识.

练习册系列答案
 字词句段篇系列答案
字词句段篇系列答案
相关题目
15. 在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂,他们对该试剂进行了定量实验分析:称取试剂15g放入锥形瓶中,加入35g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如图.请根据有关信息回答问题.
在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂,他们对该试剂进行了定量实验分析:称取试剂15g放入锥形瓶中,加入35g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如图.请根据有关信息回答问题.
(1)a的数值为125,兴趣小组的同学通过实验,得出该试剂已部分变质的结论,其依据是(通过实验数据和图象做出你的分析)滴加盐酸至100g时,开始时有二氧化碳生成,证明有碳酸钙存在,之前滴加的盐酸无现象,说明了盐酸与氢氧化钙反应,从而证明氢氧化钙存在.
(2)b的数值为2.2.
(3)计算该试剂中氢氧化钙的质量分数(写出计算过程,结果保留一位小数).
 在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂,他们对该试剂进行了定量实验分析:称取试剂15g放入锥形瓶中,加入35g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如图.请根据有关信息回答问题.
在实验室中化学兴趣小组的同学发现了一瓶敞口放置的Ca(OH)2粉末状试剂,他们对该试剂进行了定量实验分析:称取试剂15g放入锥形瓶中,加入35g的水,充分振荡,再向锥形瓶中依次滴加25g盐酸充分反应.测得部分数据与图象如图.请根据有关信息回答问题.| 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入盐酸的质量(g) | 25 | 25 | 25 | 25 | 25 | 25 |
| 锥形瓶中物质的质量(g) | 75 | 100 | a | 150 | 172.8 | 197.8 |
(2)b的数值为2.2.
(3)计算该试剂中氢氧化钙的质量分数(写出计算过程,结果保留一位小数).
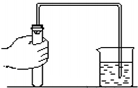 检查如图装置气密性的步骤为(1)(2)(3)(4):
检查如图装置气密性的步骤为(1)(2)(3)(4):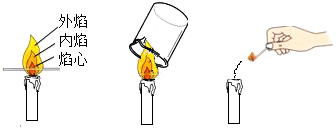
 实验室按照如图所示的装置,制取二氧化碳并检验其性质,试回答下列问题:
实验室按照如图所示的装置,制取二氧化碳并检验其性质,试回答下列问题: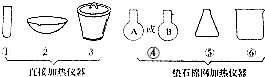
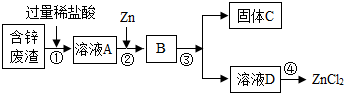 变废为宝既可避免资源浪费又可保护环境.如以含锌废濟(主要成分为Zn、ZnO、FeO、CuO)为原料可制备氯化锌,其流程如图所示.
变废为宝既可避免资源浪费又可保护环境.如以含锌废濟(主要成分为Zn、ZnO、FeO、CuO)为原料可制备氯化锌,其流程如图所示.