题目内容
5. 向100g Ca(NO3)2溶液中逐渐滴加200g K2CO3溶液.生成沉淀的质量与滴人的K2CO3溶液的质量关系如图所示.试计算:
向100g Ca(NO3)2溶液中逐渐滴加200g K2CO3溶液.生成沉淀的质量与滴人的K2CO3溶液的质量关系如图所示.试计算:(1)B点溶液中的溶质有碳酸钾和硝酸钾
(2)若在A点结束实验.则过滤后所得溶液的溶质质量分数(结果精确到0.1%).
分析 (1)根据图象可直接看出,当加入100gK2CO3溶液时,恰好反应,B点时,碳酸钾过量.故B点溶液中溶质有:碳酸钾和硝酸钾;
(2)根据图象可直接看出,当加入100gK2CO3溶液时,恰好反应,所得溶液的溶质为硝酸钾,根据化学方程式,利用沉淀的质量可求出硝酸钾的质量,进而求质量分数.
解答 解:(1)根据图象可直接看出,当加入100gK2CO3溶液时,恰好反应,B点时,碳酸钾过量.故B点溶液中溶质有:碳酸钾和硝酸钾;
(2)设硝酸钾的质量为x
K2CO3+Ca(NO3)2═CaCO3↓+2KNO3
100 202
10g x
$\frac{100}{202}=\frac{10g}{x}$
x=20.2g
过滤后所得溶液的溶质质量分数:$\frac{20.2g}{100g+100g-10g}×100%$=10.6%.
答:过滤后所得溶液的溶质质量分数为10.6%.
点评 本考点考查了根据化学方程式的计算和质量分数的计算,是考试计算题中经常出现的题型.做题时要注意:化学方程式要写正确,始终不要忘记质量守恒定律.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.以下说法正确的是( )
| A. | 中和反应有水和盐生成,有水和盐生成的反应一定是中和反应 | |
| B. | 置换反应有单质生成,有单质生成的反应一定是置换反应 | |
| C. | 碳酸盐与酸反应放出气体,与酸反应放出气体的物质不一定是碳酸盐 | |
| D. | 盐能解离出酸根离子,能解离出酸根离子的化合物一定是盐 |
20.下列实验现象描述正确的是( )
| A. | 氧化铁与稀盐酸反应,黑色固体消失,溶液由无色变成黄色 | |
| B. | 木炭在氧气中燃烧,发出白色火焰,放热,生成一种无色气体 | |
| C. | 分别点燃聚乙烯和聚氯乙烯,聚氯乙烯燃烧时产生刺激性气味气体氯化氢 | |
| D. | 硝酸铵与熟石灰研磨产生一种刺激性气味气体 |
16.下列有关溶液的说法不正确的是( )
| A. | 降低温度或增大压强均可以增大气体在水中的溶解度 | |
| B. | 物质的溶解度不一定都随温度升高而增大 | |
| C. | 在一定条件下,饱和溶液与不饱和溶液之间可相互转化 | |
| D. | 溶液中有晶体析出时,溶质质量减小,所以溶质的质量分数一定减小 |
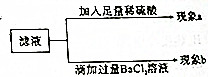 在做课本纯碱的化学性质分组实验时,第-组学生进行Na2CO3与BaC12溶液的反应,第二组学生进行Na2CO3与H2SO4溶液的反应.
在做课本纯碱的化学性质分组实验时,第-组学生进行Na2CO3与BaC12溶液的反应,第二组学生进行Na2CO3与H2SO4溶液的反应. 某固体物质由硫酸铜和氢氧化钠组成,取28g该固体溶于水后,向所得的混合物中逐滴加入10%的稀硫酸,发现沉淀量Y与稀硫酸的质量X的关系如图,求该混合物中硫酸铜和氢氧化钠的质量.
某固体物质由硫酸铜和氢氧化钠组成,取28g该固体溶于水后,向所得的混合物中逐滴加入10%的稀硫酸,发现沉淀量Y与稀硫酸的质量X的关系如图,求该混合物中硫酸铜和氢氧化钠的质量.