题目内容
11.白云岩矿(含CaO、MgO)常用于生产K2SO4肥及氮钾复合肥.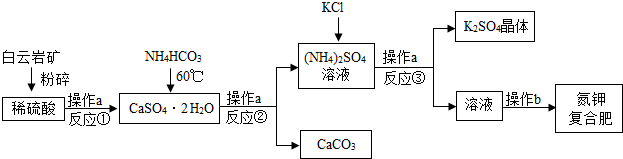
(1)将白云岩矿石粉碎的目的增大反应物的接触面积,加快化学反应速率;
(2)操作a是过滤,用到的玻璃仪器除玻璃棒还有烧杯、漏斗,玻璃棒作用引流;
(3)反应②化学方程式为CaSO4•2H2O+2NH4HCO3=CaCO3↓+(NH4)2SO4+CO2↑+3H2O,该反应温度需控制在60℃左右,原因加快该反应速率且防止碳酸氢铵受热分解;
(4)K2SO4在水中溶解度小于(NH4)2SO4,写出反应③的化学方程式(NH4)2SO4+2KCl═K2SO4↓+2NH4Cl,操作b的步骤:加热浓缩、冷却结晶、过滤而得到氮钾复合肥.
分析 (1)根据反应物的接触面积与反应速率成正比进行分析;
(2)由图框可知,操作a是过滤;
(3)碳酸氢铵受热易分解;
(4)根据题干信息来书写.
解答 解:(1)反应物的接触面积与反应速率成正比,将氧化铜矿石粉碎,增大了反应物的接触面积,加快了反应速率,白云岩矿石粉碎的目的是:增大反应物的接触面积,加快化学反应速率;故填:增大反应物的接触面积,加快化学反应速率;
(2)操作a是分离难溶性固体和液体的方法,是过滤,需要用到的玻璃仪器主要有烧杯、漏斗、玻璃棒;其中玻璃棒的作用是引流;故填:过滤;烧杯、漏斗;引流;
(3)碳酸氢铵在加热的条件下会发生分解,所以要控制温度,故填:加快该反应速率且防止碳酸氢铵受热分解;
(4)氯化钾和硫酸铵反应生成氯化铵和硫酸钾沉淀;从溶液中获得晶体,需要加热浓缩.故填:(NH4)2SO4+2KCl═K2SO4↓+2NH4Cl;加热浓缩.
点评 本题考查了制备实验方案设计,涉及知识点较多,明确物质的性质是解本题关键,明确框图的含义即可得出正确结论,同时考查学生分析问题和解决问题的能力,难度中等.

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目
1.把一块干冰放在玻璃片上,一段时间后干冰“消失”了.这一现象无法说明( )
| A. | 分子很小 | B. | 分子在不断运动 | C. | 分子间有间隔 | D. | 分子分成了原子 |
2.对化学反应:C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑的叙述中不正确的是( )
| A. | 该反应是置换反应 | B. | CO2体现氧化性 | ||
| C. | CuO体现氧化性 | D. | C体现还原性 |
19.下列关于生产、生活和能源中的化学知识不正确的是( )
| A. |  如图是“节能减排”中的节能标志 如图是“节能减排”中的节能标志 | |
| B. | 安装煤炭“固硫”装置,可降低酸雨发生率 | |
| C. | 推广农作物的生物防治技术,减少农药的使用 | |
| D. | 加快化石燃料的开采与使用 |
6.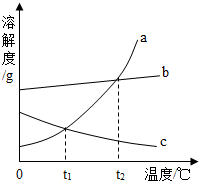 如图是a、b、c三种固体的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种固体的溶解度曲线,下列说法正确的是( )
 如图是a、b、c三种固体的溶解度曲线,下列说法正确的是( )
如图是a、b、c三种固体的溶解度曲线,下列说法正确的是( )| A. | b的溶解度一定小于a的溶解度 | |
| B. | 当b中含有少量a时,可以用蒸发结晶的方法提纯b | |
| C. | 通过升高温度可将c的饱和溶液变为不饱和溶液 | |
| D. | 将t2℃时a、b的饱和溶液降温至t1℃,析出晶体质量a一定大于b |
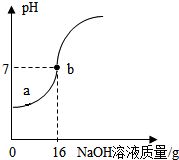 实验室欲测定一瓶标签破损的稀硫酸的溶质质量分数.现取8g稀硫酸样品,将10%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液液的pH的变化如图所示.试回答:
实验室欲测定一瓶标签破损的稀硫酸的溶质质量分数.现取8g稀硫酸样品,将10%的NaOH溶液逐滴加入到样品中,边加边搅拌,随着NaOH溶液的加入,溶液液的pH的变化如图所示.试回答: 物质王国举行一场趣味篮球赛.某队由铁、二氧化碳、硫酸、氢氧化钙、氯化铜五名“队员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成一次有效进攻.场上“队员”位置及传球路线如图所示.
物质王国举行一场趣味篮球赛.某队由铁、二氧化碳、硫酸、氢氧化钙、氯化铜五名“队员”组成,比赛中,由氯化铜“队员”发球,“队员”间传接球,最后由D位置“队员”投篮进球完成一次有效进攻.场上“队员”位置及传球路线如图所示.