题目内容
质量相等的
Mg、Zn、Fe与足量的稀盐酸反应,生成 的质量由多到少的顺序排列正确的是
的质量由多到少的顺序排列正确的是
[
]|
A .Mg>Zn>Fe |
B .Mg>Fe>Zn |
|
C .Zn>Fe>Mg |
D .Fe>Mg>Zn |
答案:B
解析:
提示:
解析:
|
解析:等质量的 Mg、Fe、Zn与足量的稀盐酸反应,放出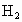 的质量的多少取决于三种金属的相对原子质量的大小,相对原子质量越大的放出 的质量的多少取决于三种金属的相对原子质量的大小,相对原子质量越大的放出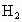 越少,相对原子质量越小的放出 越少,相对原子质量越小的放出 越多.所以生成 越多.所以生成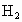 由多到少的顺序为Mg>Fe>Zn. 由多到少的顺序为Mg>Fe>Zn. |
提示:
|
点拨:此类题属常见题型,审题时应注意“等质量金属”与“足量”盐酸反应,自然产生的  质量取决于三种金属的化合价与相对原子质量,由于这三种金属与酸反应时化合价均为+2价,因此相对原子质量越大,产生 质量取决于三种金属的化合价与相对原子质量,由于这三种金属与酸反应时化合价均为+2价,因此相对原子质量越大,产生 越少,反之产生 越少,反之产生 越多. 越多. |

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目